MORANDINI, A. C. & MARQUES, A. C. (2010)
Revision of the genus Chrysaora Péron & Lesueur, 1810 (Cnidaria: Scyphozoa).
Zootaxa 2464. 97 Seiten. ISBN 978-1-86977-527-8 (paperback)ISBN 978-1-86977-528-5 (Online edition)
Abstract:
Revision of the scyphozoan genus Chrysaora Péron & Lesueur, 1810 was undertaken from observations on museum material (Brazil, Europe, and USA), on living specimens in nature, and on life-cycles of some species cultured under laboratory conditions. A total of 168 museum lots, some of them having many medusae, were inspected. Included amongst these were nine type specimens. The genus comprises 13 valid species (Chrysaora achlyos, C. chinensis, C. colorata, C.fulgida, C. fuscescens, C. hysoscella, C. lactea, C. melanaster, C. pacifica, C. pentastoma, C. plocamia, and C. quinquecirrha), one species inquirenda (Chrysaora caliparea), and two doubtful species (C. kynthia and C. wurlerra). Differentiation of species is based mostly on tentacle number, shape of radial septa, order of tentacle development,colouration, and measurements of nematocysts. We resurrect C. chinensis for specimens from southeast Asia. Chrysaora pacifica is considered valid and distinct from C. melanaster based on tentacle number and nematocyst complement. Mediterranean specimens assigned to C. hysoscella are hermaphroditic and thereby considered distinct from those of C.fulgida from west Africa. Chrysaora achlyos (northeast Pacific) and C. plocamia (southeast Pacific and southwest Atlan-tic) are geographically isolated but morphologically identical, being distinguished only by colour pattern. The recentlydescribed C. southcotti is considered a junior synonym of C. pentastoma. The Australian C. kynthia and C. wurlerra, here considered nomina dubia, merit further study Our phylogenetic hypothesis indicates that the genus Chrysaora forms a monophyletic group, with C. colorata, C. plocamia, and C. achlyos having a basal position in the phylogeny. Species with more than 24 tentacles (formerly assigned to the genus Dactylometra) form a clade with a derived position.
morandini-biblio
DE SANTANA, C. D. et al. (2019)
Unexpected species diversity in electric eels with a description of the strongest living bioelectricity generator.
Nature Communications volume 10, Article number: 4000 (2019). https://www.nature.com/articles/s41467-019-11690-z
Abstract:
Is there only one electric eel species? For two and a half centuries since its description by Linnaeus, Electrophorus electricus has captivated humankind by its capacity to generate strong electric discharges. Despite the importance of Electrophorus in multiple fields of science, the possibility of additional species-level diversity in the genus, which could also reveal a hidden variety of substances and bioelectrogenic functions, has hitherto not been explored. Here, based on overwhelming patterns of genetic, morphological, and ecological data, we reject the hypothesis of a single species broadly distributed throughout Greater Amazonia. Our analyses readily identify three major lineages that diverged during the Miocene and Pliocene—two of which warrant recognition as new species. For one of the new species, we recorded a discharge of 860 V, well above 650 V previously cited for Electrophorus, making it the strongest living bioelectricity generator.
santana-biblio; de santana-biblio
MEIK, J.M., STREICHER, J.W., LAWING, A. M., FLORES-VILLELA, O. & FUJITA, M. K. (2015)
Limitations of Climatic Data for Inferring Species Boundaries: Insights from Speckled Rattlesnakes.
PLoS ONE 10(6): e0131435. doi:10.1371/journal.pone.013143
Abstract:
Phenotypes, DNA, and measures of ecological differences are widely used in species delimitation. Although rarely defined in such studies, ecological divergence is almost always approximated using multivariate climatic data associated with sets of specimens (i.e., the “climatic niche”); the justification for this approach is that species-specific climatic envelopes act as surrogates for physiological tolerances. Using identical statistical procedures, we evaluated the usefulness and validity of the climate-as-proxy assumption by comparing performance of genetic (nDNA SNPs and mitochondrial DNA), phenotypic, and climatic data for objective species delimitation in the speckled rattlesnake (Crotalus mitchellii) complex. Ordination and clustering patterns were largely congruent among intrinsic (heritable) traits (nDNA, mtDNA, phenotype), and discordance is explained by biological processes(e.g., ontogeny, hybridization). In contrast, climatic data did not produce biologically meaningful clusters that were congruent with any intrinsic dataset, but rather corresponded to regional differences in atmospheric circulation and climate, indicating an absence of inherent taxonomic signal in these data. Surrogating climate for physiological tolerances adds artificial weight to evidence of species boundaries, as these data are irrelevant for that purpose. Based on the evidence from congruent clustering of intrinsic datasets, we recommend that three subspecies of C.mitchellii be recognized as species: C.angelensis,C.mitchellii, and C.Pyrrhus.
meik-biblio
DOUGLAS, M. E., DOUGLAS, M. R., SCHUETT, G. R. & PORRAS, L. W. (2006)
Evolution of rattlesnakes (Viperidae; Crotalus) in the warm deserts of western North America shaped by Neogene vicariance and Quaternary climate change.
Molecular Ecology (2006) 15, 3353 – 3374. doi: 10.1111/j.1365-294X.2006.03007.x
Abstract:
During Pleistocene, the Laurentide ice sheet rearranged and diversified biotic distributionsin eastern North America, yet had minimal physical impact in western North Americawhere lineage diversification is instead hypothesized to result from climatic changes. If Pleistocene climatic fluctuations impacted desert species, the latter would reflect patterns of restricted gene flow concomitant with indications of demographic bottlenecks. Accordingly, molecular evidence for refugia should be present within these distributions and for subsequent range expansions as conditions improved. We sought answers to these questions by evaluating mitochondrial DNA (mtDNA) sequences from four species of rattle-snakes [Crotalus mitchellii (speckled rattlesnake), Crotalus cerastes (sidewinder), Crotalus tigris (tiger rattlesnake), Crotalus ruber (red diamond rattlesnake)] with distributions restricted to desert regions of southwestern North America. We inferred relationships using parsimony and maximum likelihood, tested intraspecific clades for population expansions, applied an isolation-with-migration model to determine bi-directional migration rates (m) among regions, and inferred divergence times for species and clades by applying a semiparametric penalized likelihood approach to our molecular data. Evidence for significant range expansion was present in two of eight regions in two species (Crotalus mitchellii pyrrhus, C. tigris region north). Two species (C. cerastes, C. mitchellii) showed a distribution concomitant with northward displacement of Baja California from mainland México, followed by vicariant separation into subclades. Effects of Pleistoceneclimate fluctuations were found in the distributions of all four species. Three regional diversification patterns were identified: (i) shallow genetic diversity that resulted from Pleistocene climatic events (C. tigris, C. ruber); (ii) deep Pleistocene divisions indicating allopatric segregation of subclades within refugia (C. mitchellii, C. cerastes); and (iii) line-age diversifications that extended to Pliocene or Late Miocene (C. mitchellii, C. cerastes). Clade-diversifying and clade-constraining effects impacted the four species of rattlesnakes unequally. We found relatively high levels of molecular diversification in the two most broadly distributed species (C. mitchellii, C. cerastes), and lower levels of genetic diversification in the two species (C. tigris, C. ruber) whose ranges are relatively more restricted. Furthermore, in several cases, the distributions of subspecies were not congruent with our molecular information. We suggest regional conservation perspectives for southwestern deserts cannot rely upon subspecies as biodiversity surrogates, but must instead employ a molecular and deep historical perspective as a primary mechanism to frame biodiversity reserves within this region.
douglas-biblio
ARNOLD, E. N., ROBINSON, M. & CARRANZA, S. (2009)
A preliminary analysis of phylogenetic relationships and biogeography of the dangerously venomous Carpet Vipers, Echis (Squamata, Serpentes, Viperidae) based on mitochondrial DNA sequences.
Amphibia-Reptilia 30(2):273-282. DOI: 10.1163/156853809788201090.
Abstract:
Phylogenetic analysis of 1117 bp of mitochondrial DNA sequences (731 bp of cytochrome b and 386 bp of 16S rRNA) indicate that Echis consists of four main clades: E. ocellatus, and the E. coloratus, E. pyramidum, and E. carinatus groups. In the E. coloratus group, E. coloratus itself shows substantial genetic divergence from E. omanensis, corroborating their separate species status. In the E. pyramidum clade, E. pyramidum from Egypt and E. leucogaster from West Africa are genetically very similar, even though samples are separated by 4000 km. South Arabian populations of the E. pyramidum group are much better differentiated from these and two species may be present, animals from Dhofar, southern Oman probably being referable to E. khosatzkii. In the E. carinatus group, specimens of E. carinatus sochureki and E. multisquamatus are very similar in their DNA. The phylogeny indicates that the split between the main groups of Echis was followed by separation of African and Arabian members of the E. pyramidum group, and of E. coloratus and E. omanensis. The last disjunction probably took place at the lowlands that run southwest of the North Oman mountains, which are likely to have been intermittently covered by marine incursions; they also separate the E. pyramidum and E. carinatus groups and several sister taxa of other reptiles. The E. carinatus group may have spread quite recently from North Oman into its very extensive southwest Asian range, and there appears to have been similar expansion of E. pyramidum (including E. leucogaster) in North Africa. Both these events are likely to be associated with the marked climatic changes of the Pleistocene or late Pliocene. Similar dramatic expansions have also recently occurred in three snake species in Iberia.
arnold-biblio
MINTON JR., S. A. (1966)
A Contribution to the Herpetology of West Pakistan.
Bulletin of the American Museum of Natural History 134 (Article 2): 27-184.
Inhalt:
The present paper is a report on a collection of approximately 1500 amphibians and reptiles from West Pakistan and an account of natural historyo bservations made on the herpetofauna during a period of aboutfour years.A definitive herpetology of the province must await more complete zoologicale xploration and the examination of larger and more representative collections.
minton-biblio
BÖHME, W. (1977)
Eine neue Art der Gattung Bitis (SERPENTES VIPERIDAE) aus Äthiopien.
Monitore Zoologico Italiano. Supplemento, 9:1,59-68, DOI: 10.1080/03749444.1977.10736843.
Zusammenfassung:
Aus dem bewaldeten Bergland SW-Athiopiens wird Bitis parviocula n.sp. beschrieben, eine große, B. nasicornis (Schaw, 1802), B. gabonica (Dumeril, Bibron & Dumeril, 1854) und B. arietans (Merrem, 1820) nahestehende Art. Ihre Merkmale werden hinsichtlich ihrer phylogenetischen Beziehungen und einer wahrscheinlich unterirdischen Lebensweise diskutiert.
böhme-biblio
BAIG, K. J. & MASROOR, R. (2008)
The snakes of the genus Spalerosophis Jan, 1865 in Indo-Pakistan and Iran.
Herpetozoa 20:109-115
Abstract:
The present studies aimed to resolve some systematic issues related to species of the colubrid snake genus Spalerosophis JAN, 1865. The studies were carried out with particular reference to Spalerosophis atriceps FISCHER, 1885 that has been rated controversially since long among other things because of the incorrect identification of the type locality of Spalerosophis diadema (SCHLEGEL, 1837). The studies conclude that atriceps is an independent species and schirazianus is a junior synonym of Spalerosophis diadema.
baig-biblio
Rotflügelsittich
Ordnung: Papageienvögel (Psittaciformes)
Familie: Echte Papageien (Psittacidae)
Unterfamilie: Eigentliche Papageien (Psittacinae)
Tribus: Plattschweifsittiche (Platycercini)
Rotflügelsittich
Aprosmictus erythropterus • The Red-winged Parrot • La perruche érythroptère
- Körperbau und Körperfunktionen
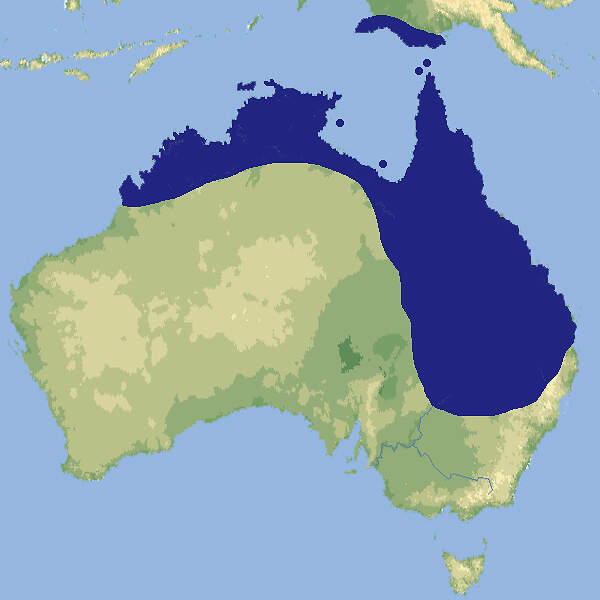
- Verbreitung
- Lebensraum und Lebensweise
- Gefährdung und Schutz
- Bedeutung für den Menschen
- Haltung
- Taxonomie und Nomenklatur
- Literatur und Internetquellen
|
Weitere Bilder auf BioLib.czStimme auf XENO-CANTO |
Der in seiner Heimat nicht gefährdete, aber aufgrund nationaler Gesetzgebung seit Langem nicht mehr exportierte Rotflügelsittich ist weist einen Geschlechtsdichromatismus auf der allerdings nicht so eklatant ist wie beim recht ähnlichen Königssittich. Er wird in Zoos auch nicht so häufig gehalten wie jener. Körperbau und KörperfunktionenDer Rotflügelsittich erreicht eine Gesamtlänge von 30-32 cm, wovon 14-15 cm auf den breiten Schwanz entfallen, eine Flügellänge von 18-21 cm und ein Gewicht von im Mittel etwa 160 (120-210) g. Es besteht ein deutlicher Dichromatismus zwischen den Geschlechtern: Das Gefieder der Hähne ist überwiegend grasgrün. Der Oberrücken ist schwarz, die mittleren großen Flügeldecken sind rot, die Flügel ansonsten dunkelgrün. Bei den Hennen fehlt der schwarze Oberrücken, und der rote Bereich auf dem Flügel ist deutlich kleiner. Bei beiden Geschlechtern ist die Iris orangerot und sind die Füße grau. Der Schnabel ist beim Männchen korallenrot, beim Weibchen blassrot [1; 5; 6; 7]. VerbreitungAustralasien: Im Norden und Osten Australiens, Indonesien (West-Papua), Papua-Neuguinea [2]. Lebensraum und LebensweiseDer Rotflügelsittich besiedelt vorzugsweise lichte Monsun- und Trockenwälder der Tropen und Subtropen, Savannen und Akazien-Trockenbusch. Das Nahrungsspektrum ist vielfältig und schließt Samen von Eukalypten, Akazien, Wildhopfen (Dodonea) und anderen Bäumen, Grassamen, Früchte, Beeren, Mistelbeeren (Loranthus), Knospen, Blüten, Nektar und Insekten ein. Die Vögel werden in der Regel paarweise oder in kleinen Gruppen, selten in Schwärmen bis zu 60 Individuen angetroffen. Genistet wird in meist sehr tiefen Baumhöhlen, vorzugsweise in Eukalypten. Das Gelege besteht aus 3-5(-6) Eiern, die während 18-20 Tagen allein vom Weibchen bebrütet werden. Die Nestlingsdauer beträgt ca. 35 Tage [1; 6; 7]. Gefährdung und SchutzDer Rotflügelsittich hat eine sehr weite Verbreitung und gilt als häufig. Der Bestand nimmt vermutlich zu. Deshalb ist die Art seit 2004 als nicht-gefährdet eingestuft (Rote Liste: LEAST CONCERN) [2]. Der internationale Handel ist nach CITES Anhang II geregelt. Bedeutung für den MenschenRotflügelsittiche werden im Ursprungsgebiet als Heimtiere gefangen bzw. ausgehorstet [2]. Von 1981-2018 meldete Australien keine Exporte von Wildfängen, sondern nur die Ausfuhr eines Nachzuchtvogels. Im selben Zeitraum wurden weltweit 4'706 Nachzuchtvögel bei der Ausfuhr registriert. Davon stammten 1'710 aus den Niederlanden [4]. HaltungDie Haltung erfolgt am besten paarweise in Volieren von 4-5 m Länge mit anschließendem, im Winter leicht temperiertem Schutzhaus. Das Höchstalter wird mit 27 Jahren und 4 Monaten angegeben. Im Tiergarten Schönbrunn erreichte ein Vogel 24 Jahre und 5 Monate. Die Erstzucht in Menschenobhut gelang 1878 in Deutschland [1; 3; 8]. Haltung in europäischen Zoos: Bereits 1861 war der Rotflügelsittich im Londoner Zoo zu sehen: Heute (2022) wird die Art in rund 50 Zoos gezeigt, von denen sich über ein Drittel im deutschsprachigen Raum befinden. Für Details siehe Zootierliste. Mindestanforderungen an Gehege: Nach Papageiengutachten des BMELF von 1995 ist für die Haltung eines Paars oder ausnahmsweise eines Einzelvogels eine Voliere mit einer Grundfläche von 3 m² und einer Höhe von 2 m erforderlich, ferner ein Schutzraum mit einer Grundfläche von 2 m². Für jedes weitere Paar sind die Grundflächen um 50% zu erweitern. Die in der Schweizerischen Tierschutzverordnung (Stand 1.2.2022) enthaltenen Mindestanforderungen für Sittiche sind für Rotflügelsittiche nicht vertretbar. Die 2. Tierhaltungsverordnung Österreichs (Stand 2022) schreibt für die Haltung eines Paars oder ausnahmsweise eines Einzelvogels eine Voliere mit einer Grundfläche von 4 x 2 m Fläche und einer Höhe von 2 m sowie einen frostfreien Schutzraum von 2 m² / 1 m Höhe vor. Je weiteres Paar sind die Flächen um 50% zu erweitern. Taxonomie und NomenklaturDer Rotflügelsittich wurde 1788 vom Göttinger Professor Johann Friedrich GMELIN in der von ihm bearbeiteten 13. Auflage von LINNÉS "Systema Naturae" als "Psittacus erythropterus" erstmals wissenschaftlich beschrieben. Die heute gültige Gattungsbezeichnung Aprosmictus wurde 1848 von dem englischen Ornithologen und Illustrator John GOULD eingeführt. Es werden gegenwärtig drei Unterarten anerkannt [6]:
|
Literatur und Internetquellen
- ASMUS, J. & LANTERMANN, W. (2012)
- BIRDLIFE INTERNATIONAL (2016). Aprosmictus erythropterus. The IUCN Red List of Threatened Species 2016: e.T22685069A93057458. https://dx.doi.org/10.2305/IUCN.UK.2016-3.RLTS.T22685069A93057458.en . Downloaded on 17 April 2020.
- BROUWER, K., JONES, M. L., KING, C. E. und SCHIFTER, H. (2000)
- CITES TRADE DATA BASE
- DE GRAHL, W. (1982)
- DEL HOYO, J., ELLIOTT, A. et al. (eds., 1992-2013)
- GRUMMT, W. & STREHLOW, H. (2009)
- YOUNG, A. M., HOBSON, E. A., BINGAMAN LACKEY, L. & WRIGHT, T. F. (2012)
Zurück zu Papageienvögel (PSITTACIFORMES)
Weiter zu Edelpapagei (Eclectus roratus)
DONNDORFF, J. A. (1792)
Zoologische Beyträge zur XIII. Ausgabe des Linnéischen Natursystems.
Erster Band: Die Säugethiere.
919 Seiten. Verlag der Weidmannschen Buchhandlung Leipzig.
Facsimile: https://www.biodiversitylibrary.org/bibliography/44569#/summary
donndorff-biblio