MARKOWSKI, S. (2013)
Tierart- und erregerspezifische Maßnahmen zur Optimierung des Gesundheitsmanagements für nordamerikanische Säugetiere in Zoologischen Gärten.
Vet.med. Diss Hannover.
Wissenschaftliche Betreuung : Prof. Dr. Michael Böer, Institut für Tierhygiene, Tierschutz und Nutztierethologie
312 Seiten.
Ziel der Arbeit war es, durch Auswertung von 5389 Untersuchungsfällen bei acht nordamerikanischen Tierarten in Zoologischen Gärten, ergänzt durch entsprechende Literaturstudien, die wichtigsten bakteriologischen, parasitologischen und virologischen Infektionserreger zu bestimmen, um entsprechende tiermedizinische Überwachungs – und Kontrollprogramme zu optimieren.
Mit den Ergebnissen der Literaturstudie lassen sich bedeutende Erreger bei den untersuchten Tierarten eingrenzen. Häufig traten verschiedene Enterobacteriaceae, bei Wölfen, Luchsen und Elchen auch Salmonellainfektionen, auf. Ebenfalls zahlreich waren Clostridien, Brucellainfektionen und Leptospirosen, bei Robben auch Streptokokkeninfektionen dokumentiert. Dominierende parasitäre Infektionen waren durch Askaridoidea, Ankylostomatoidea, Strongyloidea, Tricho- und Metastrongyloidea sowie Trichuris bei den Elchen induziert. Cestodainfektionen waren vor allem bei Luchs und Wolf, Trematodanachweise bei Bibern und Wölfen beschrieben. Zu den bedeutenden in der Literatur genannten Virusinfektionen zählen vor allem Distempervirusinfektionen. Ebenfalls häufig traten Parvo – und Tollwutvirusinfektionen auf. Bei den Hirschen dominierten Infektionen mit Erregern des Katarrhalfiebers, der Bovinen Virusdiarrhoe sowie mit dem Bovinen Herpesvirus 1.
Die Auswertung der 5389 Untersuchungsfälle zeigte, dass bei allen acht beteiligten Tierarten Vertreter der Enterobacteriaceae in großer Zahl den größten Anteil der nachgewiesenen Bakterien ausmachten. Ebenfalls häufig waren Streptokokken und Clostridien dokumentiert. Ähnlich den Ergebnissen der Literaturstudie wurden Askaridoidea und Trichuris (bei den Elchen) als wichtige parasitologische Erreger identifiziert. Staupevirusinfektionen traten am häufigsten bei Robben auf, Parvovirusinfektionen bei Wölfen und Luchsen. Das Virus der Bovinen Virusdiarrhoe wurde für beide Hirscharten nachgewiesen. Bei Elchen wurden Infektionen mit einem Erreger des Katarrhalfiebers, bei Rentieren mit dem Bovinen Herpesvirus 1 und Rotaviren dokumentiert. Für Biber besaßen Virusinfektionen eine untergeordnete Bedeutung, für Bären erfolgte in keinem Untersuchungsfall ein positiver Virusnachweis.
markowski-biblio
DOLLINGER, P. (1971)
Tod durch Verhalten bei Zootieren.
Death through behaviour in zoo animals.
Vet. med. Diss. Zürich.
Juris Verlag Zürich. 229 Seiten, 26 Tabellen, 11 Grafiken, 15 Fotos
Tierpsychologische Abteilung des Zoologischen Instituts, Prof. Dr. H. Hediger, und
Veterinär-Pathologisches Institut, Prof. Dr. H. Stünzi, der Universität Zürich
Zoo Zürich
Zusammenfassung:
Die vorliegende Arbeit befasst sich mit dem von HEDIGER (1956) geschaffenen Begriffs des Todes durch Verhalten (TdV) bei Zootieren. Dieser Terminus wird erstmalig definiert, wobei zwischen direktem und indirektem TdV unterschieden wird (pp. 13-14).
Aus der Literatur werden Angaben über die Häufigkeit der traumatischen Todesursachen – welche sich weitgehend mit den direkt durch Verhalten verursachten Todesfällen decken – in verschiedenen Zoos und aus verschiedenen Pathologischen Instituten zusammengestellt (pp. 15-23).
Um sichere Anhaltspunkte über die Bedeutung des TdV zu erhalten, wurden die Todesfälle im Säugetier-, Vogel- und Reptilienbestand des Zürcher Zoos von 1954-1969 bearbeitet (pp.24-47). Dabei zeigte es sich, dass über die Frequenz des indirekten TdV retrospektiv nichts ausgesagt werden kann, dass jedoch der direkte TdV bei Säugetieren und Vögeln die wichtigste Todesursache darstellt (23.4 resp. 29.4 % der Todesfälle), während er bei Reptilien relativ unbedeutend ist.
Eine Zusammenfassung der Ergebnisse aus dem Zürcher Zoo findet sich auf Seite 48.
Den breitesten Raum nimmt eine analytische Untersuchung über das Phänomen des TdV ein (pp. 49-152). Es wird ein Schema der am TdV beteiligten psychologischen, ökologischen, ethologischen und pathologischen Komponenten gegeben (p.49) und deren Beziehungen untereinander werden anhand einiger exemplarischer Beispiele dargestellt (pp. 49-53).
Anschliessend wird detailliert auf die einzelnen Komponenten eingegangen, wobei auf die auslösenden Faktoren (psychologische und ökologische Momente) besonderes Gewicht gelegt wird, da deren Kenntnis Voraussetzung und bester Ansatzpunkt für eine wirksame Prophylaxe des TdV ist (pp- 53-126).
Von den zum Tod führenden Verhaltensweisen (pp. 127-144) werden Automutilation, Inanition und Kannibalismus sowie das Syndrom des Ausbrechens, Ausreissens und Entweichens näher untersucht.
Die den Tod bewirkenden Läsionen und Funktionsstörungen werden nur der Vollständigkeit halber gestreift (pp. 144-152) und schliesslich werden noch einige grundsätzliche Bemerkungen zur Prophylaxe des TdV gemacht (pp. 153-156).
Den Abschluss des Textteils bildet die umfangreiche Kasuisitik aus den Zoos von Zürich und Mulhouse (pp.157-196) und die Bibliographie (pp. 200-216).
Abstract:
The problem of “death through behaviour” (death caused by effects of behaviour) of zoo animals (HEDIGER,l 1956) is discussed in the present paper.
A definition of this term is provided recognising direct and indirect cause of death through behaviour (pp. 13-14).
Reports from various pathology-laboratories and zoos dealing with traumatic deaths which could be contributed to animal behaviour are reviewed (pp. 15-23).
In order to emphasize the importance of above phenomenon, deaths of mammals, birds and reptiles which occurred at Zurich zoo between 1954 and 1969 were analysed (pp.24-47). The frequency of deaths caused indirectly through behaviour could not be recognised. Behaviour as direct cause of death occurred most frequently in mammals and birds (23.4 and 29.4 % respectively), but was relatively unimportant in reptiles.
The results of the survey from Zurich zoo are summarized on page 48.
The phenomenon of death through behaviour is analysed (pp. 49-152). The psychological, ethological, ecological and pathological factors and their interrelations participating in the occurrence of deaths through behaviour are illustrated on a scheme with some practical examples (pp. 49-53).
All components are discussed each in detail with particular attention to the triggering factors (psychological and ecological moments) in order to gain knowledge and basis for prophylaxis (pp- 53-126).
Some behavioural pattern leading to death, such as automutilation, inanition, cannibalism and also the occurrence of break-outs, tearings and escapes are discussed (pp. 127-144).
The lesions and functional disturbances were only briefly noted (pp. 144-152) and general remarks are given on prophylaxis (pp. 153-156).
In the final chapter case histories are listed from the zoos of Zurich and Mulhouse/France (pp.157-196) and references of the literature are provided (pp. 200-216).
dollinger-biblio
Buschbock
Überordnung: LAURASIATHERIA
Taxon ohne Rang: CETARTIODACTYLA
Ordnung: Paarzeher (ARTIODACTYLA)
Unterordnung: Wiederkäuer (Ruminantia)
Familie: Hornträger (Bovidae)
Unterfamilie: Echte Rinder (Bovinae)
Tribus: Afrikanische Waldböcke (Tragelaphini)
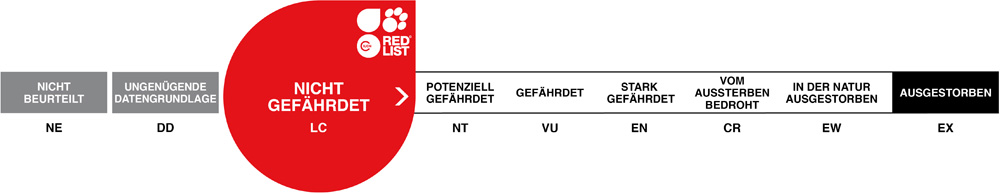
Buschbock oder Schirrantilope
Tragelaphus scriptus • The Bushbuck • Le guib harnaché
- Körperbau und Körperfunktionen
- Verbreitung
- Lebensraum und Lebensweise
- Gefährdung und Schutz
- Bedeutung für den Menschen
- Haltung
- Taxonomie und Nomenklatur
- Literatur und Internetquellen
|
Weitere Bilder auf BioLib.cz |
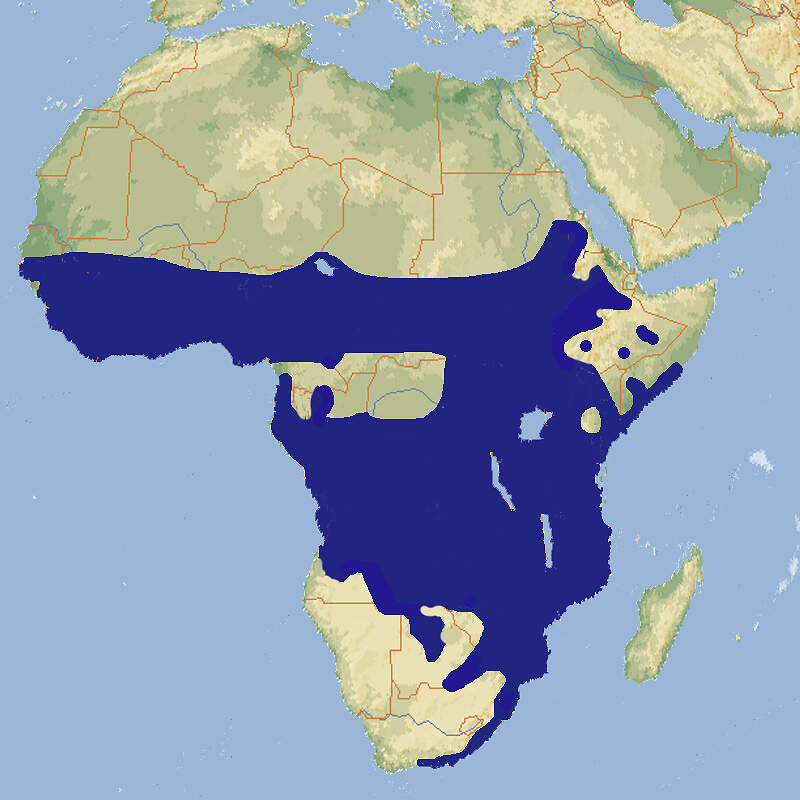
Der Buschbock ist eine kleinere, äußerst attraktive Antilope mit deutlichem Sexualdimorphismus, die sowohl für das allgemeine Publikum als auch für die Zoopädagogik interessant wäre, die aber als weit verbreitete, nicht gefährdete Art vom Europäischen Zoo- und Aquarienverband als nicht prioritör eingestuft wurde und daher in den Zoos mittlerweile ausgestorben ist. Körperbau und KörperfunktionenDer Buschbock ist der kleinste der afrikanischen Waldböcke. Er zeigt einen stark ausgeprägten Sexualdimorphismus. Die Böcke erreichen eine Kopf-Rumpflänge von 114-150 cm, eine Schulterhöhe von 80 (65-100) cm und ein Gewicht von 40-80 kg. Die Ricken werden bis 132 cm lang, 70 (61-85) cm hoch und 24-60 kg schwer. Der Schwanz wird etwa 19-24 cm lang. Wie bei den anderen afrikanischen Waldböcken haben die Böcke schraubenartig gedrehte Hörner, die 40-55 cm lang werden können. Das Fell zeigt bei beiden Geschlechtern ein auffallendes Muster weißer Punkte und Streifen, wobei es erhebliche regionale Unterschiede gibt. An der Halsunterseite verlaufen 1-2 weiße Querbänder, die Schwanzunterseite ist weiß, die Schwanzspitze kann schwarz sein. Die Beine können je nach Unterart einfarbig sein oder eine weiß oder schwarzweiße Zeichnung aufweisen. Die Grundfarbe ist regional variabel, bei den Ricken meist rotbraun, bei den Böcken etwas dunkler, kastanienbraun oder schwarzgrau [2; 5; 8]. VerbreitungAfrika südlich der Sahara: Angola, Äquatorialguinea, Äthiopien, Benin, Botswana, Burkina Faso, Burundi, Elfenbeinküste, Gabun, Gambia, Ghana, Guinea, Guinea-Bissau, Kamerun, Kenia, Kongo, Kongo Dem., Liberia, Malawi, Mali, Mauretanien, Mosambik, Namibia, Niger, Nigeria, Ruanda, Sambia, Senegal, Sierra Leone, Simbabwe, Somalia, Südafrika, Südsudan, Sudan, Swasiland, Tansania, Togo, Tschad, Uganda, Zentralafrikanische Republik [4]. Lebensraum und LebensweiseBuschböcke benötigen Lebensraum mit viel Deckung. Sie kommen in Tropischen Regen- und Feuchtwäldern, Subtropischen Feuchtwäldern, und Gemäßigten immergrünen Feuchtwäldern, jeweils vorzugsweise an Waldrändern, Galeriewäldern, Trockenwäldern, Dornsavannen, Dickichten und Zuckerrohrpflanzungen vor. Die Nahrung dieser Selektiväser besteht überwiegend aus Blättern und Zweigen, aber auch zarte Gräser werden genommen. Buschböcke leben solitär, sind aber nicht territorial, sondern haben überlappende Streifgebiete [5; 8]. Es gibt keine definierte Fortpflanzungsperiode, allenfalls saisonale Spitzen der Brunftaktivitäten und der Geburten. Nach einer Tragzeit von rund 180 Tagen wird in der Regel ein einzelnes Kitz mit einem Gewicht von 3.1-4.5 kg geboren. Angaben über das Erreichen der Geschlechtsreife sind widersprüchlich. Bei Ricken dürfte dies mit etwa 1 Jahr der Fall sein, bei Böcken mit 1.5 Jahren, wobei sie effektiv meist erst mit 3 Jahren zur Forspflanzung kommen [5; 6; 8]. Gefährdung und SchutzDer Buschbock hat eine sehr weite Verbreitung und einen geschätzten Bestand von 1 bis 1.5 Millionen Adulttieren, der als stabil angesehen wird, außer in vom Menschen dicht besiedelten Regionen. Möglicherweise ist diese Schätzung wegen der heimlichen Lebensweise des Buschbocks zu tief. Er gilt daher seit 1996 als nicht gefährdet (Rote Liste: LEAST CONCERN) , was im Rahmen einer Beurteilung aus dem Jahr 2016 bestätigt wurde. Der Klimawandel macht der Art in den trockeneren Teilen ihres Areals zu schaffen, andererseits kann sie ihre Verbreitung im Gebiet der Regenwälder ausdehnen [4]. Der internationale Handel ist nicht unter CITES geregelt. Die Einfuhr lebender Exemplare aus den Ursprungsländern ist wegen der restriktiven Veterinärbestimmungen der EU so gut wie ausgeschlossen. Bedeutung für den MenschenDer Buschbock wird zur Gewinnung von Fleisch und als Sport gejagt. In Ruanda ist sein Fleisch deutlich billiger als jenes von Nutztieren und dementsprechend ist der Buschbock die häufigste Wildtierart, die auf Fleischmärkten angeboten wird. Im Rahmen der Sportjagd werden in Südafrika "Trophy Fees" von etwa 1'200-1'500 USD fällig, in anderen afrikanischen Ländern 400-1'100 USD. HaltungIn den 1950er Jahren wurde im Zoo Basel ein Buschbock kurze Zeit gemeinsam mit Sitatungas und Vierhornantilopen gehalten, um 1990 in Hannover gemeinsam mit Kirk-Dikdiks. Eine Gemeinschaftshaltung mit Sitatungas sollte sollte wegen der Gefahr der Bastardierung tunlichts vernieden werden Als Höchstalter gibt WEIGL über 15 Jahre und 3 Monate für ein im Ruhr-Zoo Gelsenkirchen geborenes und später in Hannover gehaltenes gehaltenes weibliches Tier an [7]. Haltung in europäischen Zoos: Die Art ist dem Collection Planning der EAZA zum Opfer gefallen und wird heute nicht mehr gehalten. Die britische (europäische?) Erstzucht gelang 1841 in der Menagerie des Earl of Derby in Knowsley (heute Safaripark). Der letzte Hinweis auf eine Nachzucht in Europa im International Zoo Yearbook bezieht sich auf das Jahr 1991 (Zoo Hannover). Bei den in Europa gehaltenen Tiere handelte es sich hauptsächlich um Senegal-Buschböcke, die z.B. in Hannover 31 Jahre lang gehalten und regelmäßig gezüchtet wurden, seltener um Kap-Buschböcke. Andere Unterarten waren Ausnahmeerscheinungen. Für Details siehe Zootierliste. Mindestanforderungen an Gehege: Nach Säugetiergutachten 2014 des BMEL soll für bis zu 5 Tieren ein Gehege von mindestens 200 m² zur Verfügung stehen. Für jedes weitere Tier kommen 20 m² zur Basisfläche dazu. Zudem wird ein Stall von etwa 3 m²/Tier vorgegeben. Die Schweizerische Tierschutzverordnung (Stand 01.06.2022) schreibt für theoretisch bis zu 10 Tieren ein Gehege mit Trenn- oder Absperrmöglichkeit vor, dessen Grundfläche 500 m² misst. Für jedes weitere Tier kommen 40 m² zur Basisfläche dazu. Ferner ist ein Stall mit einer Fläche von 4 m²/Tier erforderlich. Nach der 2. Tierhaltungsverordnung Österreichs (Stand 2023) ist für 1-5 Tiere ein Außengehege von 500 m² erforderlich, für jedes weitere 50 m² mehr. Zudem ist ein beheizter Stall mit einem Mindestausmaß von 4 m² pro Tier mit einer Mindesttemperatur von 10°C vorgeschrieben. Die Haltung hat in Gruppen mit einem erwachsenen Männchen, mehreren Weibchen und deren Nachwuchs zu erfolgen. Taxonomie und NomenklaturDer Buschbock wurde 1766 vom Berliner Naturforscher Peter Simon PALLAS, den Katharina die Große als Professor nach Petersburg berufen hatte, als "Antilope scripta" anhand eines Exemplars aus dem Senegal erstmals wissenschaftlich beschrieben. 1816 stellte ihn der französische Zoologe Henri Marie Ducrotay de BLAINVILLE als Typusart in die neue Gattung Tragelaphus. Traditionell wurde die Art in über 20 (bis etwa 40) Unterarten aufgeteilt. 2005 waren es noch 9. GROVES & GRUBB splitteten in ihrer umstrittenen Huftier-Taxonomie den Buschbock in 8 Arten auf, was Eingang in das Handbuch der Säugetiere fand, aber von der IUCN im Rahmen der Roten Liste nicht mitgemacht wurde [1; 3; 4, 8; 9].
|
Literatur und Internetquellen
- GROVES, C.P. & GRUBB, P. (2011)
- GRZIMEK, B. (ed., 1970)
- HALTENORTH, T. & TRENSE, W. (1956)
- IUCN SSC Antelope Specialist Group 2016. Tragelaphus scriptus (errata version published in 2017). The IUCN Red List of Threatened Species 2016: e.T22051A115165242. http://dx.doi.org/10.2305/IUCN.UK.2016-3.RLTS.T22051A50196111.en. Downloaded on 24 March 2019.
- MILLS, G & HES, L. (1999)
- PUSCHMANN, W., ZSCHEILE, D., & ZSCHEILE, K. (2009)
- WEIGL, R. (2005)
- WILSON, D. E. et al. eds. (2009-2019)
- WILSON, D. E. & REEDER, D. M. (2005)

Weiblicher Buschbock Tragelaphus scriptus sylvaticus) in seinem natürlichen Lebensraum im Pilanesberg-Nationalpark © Peter Dollinger, Zoo Office Bern
Zurück zu Übersicht Paarzeher
Weiter zu Sitatunga (Tragelaphus spekii)
BMEL (2014)
Gutachten über Mindestanforderungen an die Haltung von Säugetieren vom 7. Mai 2014.
298 Seiten, einschließlich der Differenzprotokolle der Vertreter der Tier- und Naturschutzverbände, sowie der Vertreter der Zooverbände. Herausgeber: Bundesministerium für Landwirtschaft.
Das Gutachten füllt die zum Teil unbestimmten Rechtsbegriffe des Tierschutzgesetzes betreffend die Haltung von Säugetieren wildlebender Arten aus.
bmel-biblio
Kloakentiere - Allgemeines
Klasse: Säugetiere (Mammalia)
Unterklasse: Ursäuger (Prototheria)
Ordnung:
Kloakentiere
Monotremata • The Monotremes • Les monotrèmes
- Artenspektrum und innere Systematik
- Körperbau und Körperfunktionen
- Verbreitung
- Haltung im Zoo
- Taxonomie und Nomenklatur
- Literatur und Internetquellen
|
|
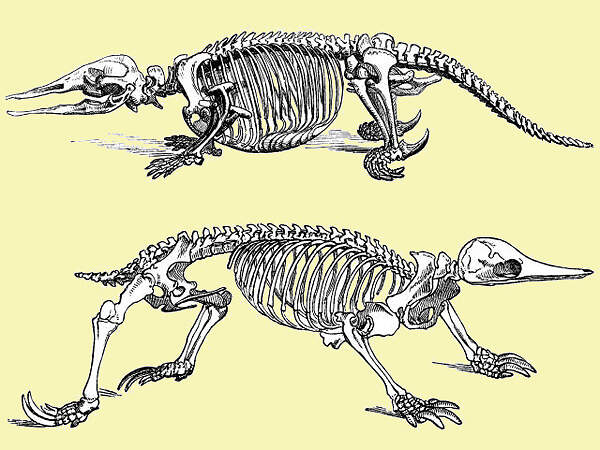
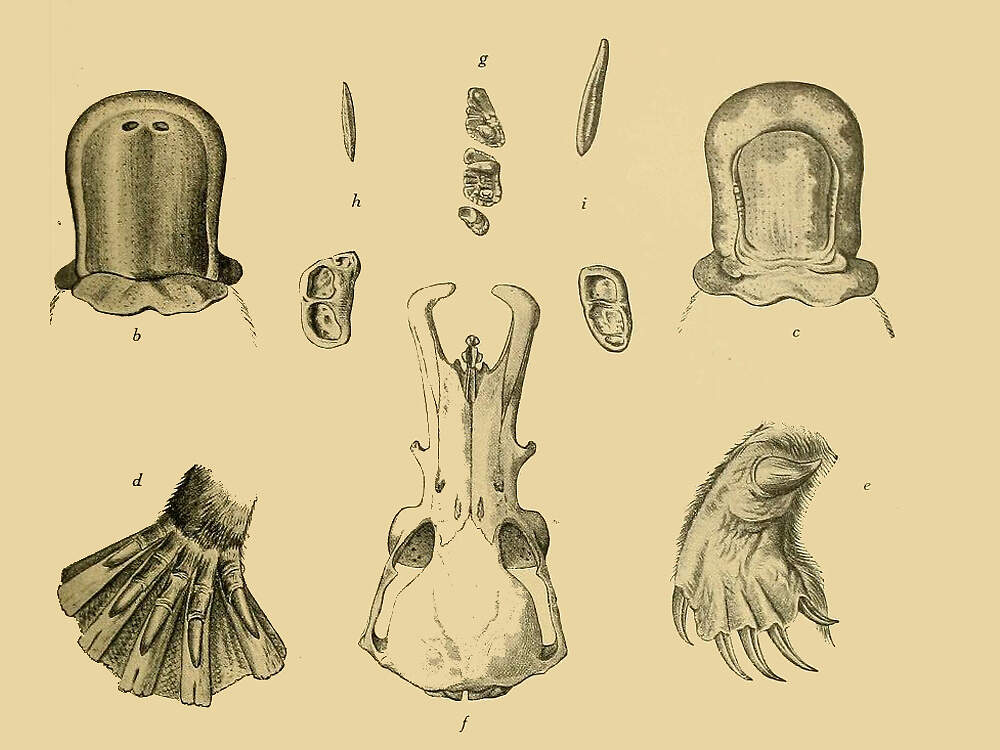
Die Kloakentiere sind primitive Säugetiere, die als einzige Eier legen. Ihr Ordnungsname weist darauf hin, dass Kot, Urin und Nachwuchs nicht wie bei anderen Säugetieren durch verschiedene Körperöffnungen nach außen gelangen, sondern dass es dafür, wie bei den Vögeln und Reptilien, nur eine gibt: die Kloake. Artenspektrum und innere SystematikDie Ordnung umfasst die Familie der Schnabeltiere (Ornithorhynchidae) mit nur einer Art sowie die Familie der Schnabeligel (Tachyglossidae) mit 2 Gattungen und 4 Arten [4]. Von diesen fünf Arten gelten zwei als vom Aussterben bedroht (Rote Liste: CRITICALLY ENDANGERED), eine als gefährdet (VULNERABLE) und eine als potenziell gefährdet (NEAR THREATENED) [2]. Körperbau und KörperfunktionenDas Skelett der Kloakentiere weist etliche Merkmale auf, die für Reptilien typisch sind, so z.B. ein großes selbständiges Rabenbein (Coracoid) und Nebenrabenbein (Epicoracoid) im Schultergürtel. Zwischen ihren Haaren bzw. Stacheln befinden sich Papillen, die den Schuppen der Reptilien entsprechen. Ihre Körpertemperatur beträgt rund 30°C. Ihr Großhirn ist nicht oder nur wenig gefurcht. Der Magen ist drüsenlos, bei den Nieren gibt es keine Mark- und Rindenzone. Statt ausgebildeter Zähne haben sie als Erwachsene einen Schnabel mit Hornplatten, mit denen sie ihre Nahrung zerkauen können. Die Harnwege und der Eileiter münden in eine Kloake, der Penis ist ausschließlich samenführend. Die Weibchen der Schnabeltiere haben in der Bauchgegend ein zitzenloses Milchdrüsenfeld, das etwa 120 Öffnungen aufweist. Die Schnabeligel haben einen Brutbeutel, in dem die Eier ausgebrütet und die Jungen mit Milch versorgt werden. Die Männchen haben am Hinterfuß einen hohlen Sporn, über den bei den Schnabeltieren Gift ausgeschieden werden kann. Die Eier haben eine Keratinschale. Die Jungen schlüpfen nach einer Brutdauer von 7-12 Tagen mit Hilfe eines Eizahns [1; 5; 7]. VerbreitungAustralien und Neuguinea. Haltung im ZooSchnabeltiere (Ornithorhynchus anatinus) wurden, wenn überhaupt, in Europa nur bis zum Ersten Weltkrieg gehalten. Versuche des englischen Zoologen Edward Turner BENNETT in den Jahren 1832 und 1858, Schnabeltiere lebend nach Europa zu bringen, scheiterten jedenfalls [7]. London und Moskau hielten als einzige europäische Zoos nach dem Zweiten Weltkrieg bis 1994 bzw. 2013 Langschnabeligel (Zaglossus spp.) Einzig Kurzschnabeligel (Tachyglossus aculeatus) werden mit einiger Regelmäßigkeit in europäischen Zoos gehalten und gelegentlich auch gezüchtet [6]. Taxonomie und NomenklaturDie systematische Einordnung des Schnabeltiers, welches als erste Monotremen-Art durch die Wissenschaft entdeckt wurde bereitete vorerst Mühe. Die ersten Bälge, welche nach England gelangten, wurden für Artefakte eines Schwindlers gehalten, der das Fell eines großen Maulwurfs mit den Freßwerkzeugen einer Ente kombiniert hatte. Dann wurde vermutet, dass es sich um eine eigenständige Tierklasse handeln könnte. Nachdem anatomische Untersuchungen das Vorhandensein von Milchdrüsen ergeben hatten, war klar, dass es sich um Säugetiere handelt, die bald den Beuteltieren, bald den Zahnarmen zugeordnet wurden. Heute werden die Kloakentiere als Unterklasse Ursäuger (Prototheria) den Beutelsäugern und Höheren Säugetieren gegenüber gestellt. Sie besteht aus nur einer Ordnung [1; 3; 7]. |
Literatur und Internetquellen
- GRZIMEK, B. (1970). In GRZIMEKs TIERLEBEN.
- IUCN Red List of Threatened Species. Version 2022-2. Downloaded on 6 January 2023.
- SIMPSON, G. G. (1945)
- WILSON, D. E. et al. eds. (2009-2019)
- ZISWILER, V. (1976)
- ZOOTIERLISTE
- BREHM, A. E. (1882-1887)
Zurück zu Kloaken- und Beuteltiere
Weiter zu Kurzschnabeligel (Tachyglossus aculeatus)
Beuteltiere - Allgemeines
Klasse: Säugetiere (Mammalia)
Unterklasse: Beutelsäuger (Metatheria)
oder:
Beuteltiere
Marsupialia • The Marsupials • Les marsupiaux
- Artenspektrum und innere Systematik
- Körperbau und Körperfunktionen
- Verbreitung
- Haltung im Zoo
- Taxonomie und Nomenklatur
- Literatur und Internetquellen
|
|
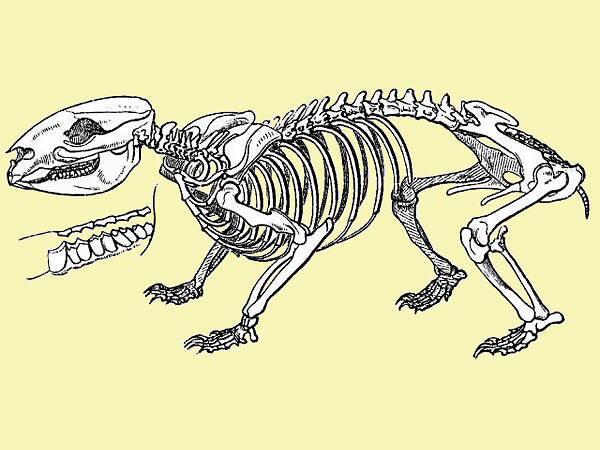
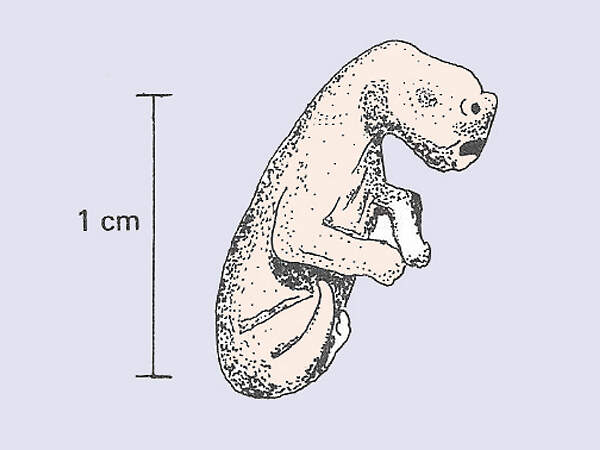
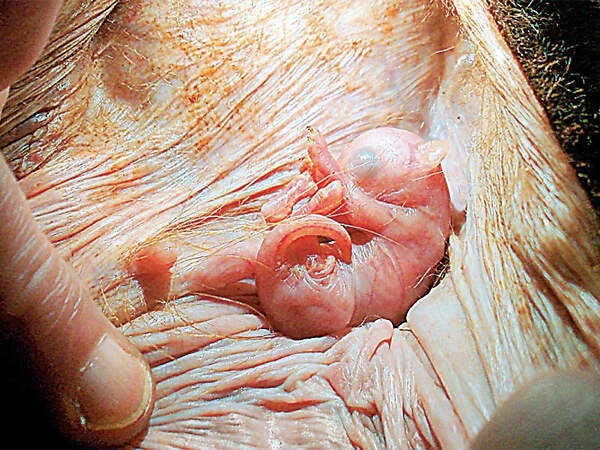
Die Beuteltiere gebären Junge, die sich noch in einem embryonalen Zustand befinden und nach der Geburt in einem Bauchbeutel fertig ausgetragen werden. Ihre Wege und die der Höheren Säugetiere haben sich zu Ende der Jurazeit – vor rund 150 Millionen Jahren - getrennt. In der nachfolgenden Evolution kam es zu zahlreichen konvergenten Entwicklungen bei den beiden Tiergruppen, z.B: Mäuse / Beutelmäuse, Goldmulle / Beutelmulle, Marder / Beutelmarder, Dachse / Beuteldachse, Wölfe / Beutelwölfe, Gleithörnchen / Gleitbeutler. Artenspektrum und innere SystematikHeute werden die 349 gegenwärtig anerkannten rezenten Arten wie folgt auf sieben Ordnungen verteilt [2; 4]:
13 Arten sind seit der Besiedlung Australiens durch die Europäer ausgestorben, 12 davon im Lauf des 20. Jahrhunderts. Eine davon, der Beutelwolf (Thylacinus cynocephalus), repräsentierte eine eigene Familie. Bei den übrigen handelt es sich um 8 Kängurus, 3 Nasenbeutler sowie ein Opossum aus Argentinien [2]. Nach Roter Liste der IUCN gelten 17 der noch lebenden Arten als vom Aussterben bedroht (CRITICALLY ENDANGERED), 22 als stark gefährdet (ENDANGERED), 43 als gefährdet (VULNERABLE) und 41 als potenziell gefährdet (NEAR THREATENED). 194 sind nicht gefährdet (LEAST CONCERN) und 19 können mangels Daten nicht eingestuft werden [2]. Körperbau und KörperfunktionenDas Skelett der Beuteltiere ist säugetiertypisch. Das Rabenbein (Coracoid) ist zwar embryonal angelegt, verschmilzt dann aber mit dem Schulterblatt. In der Regel sind Schlüsselbeine vorhanden. Als Besonderheit ist bei beiden Geschlechtern in der Gegend des Schambeins ein Paar Beutelknochen (Ossa marsupialia) ausgebildet. Die Körpertemperatur ist mit 34-36°C höher als die der Kloakentiere, aber liegt unter jener der Höheren Säugetiere. Ihr Gehirn ist klein und einfach gebaut, die Großhirnhemisphären sind praktisch ungefurcht und überlappen das Kleinhirn nicht. Gut ausgebildet ist das Riechhirn. Das Gebiss kann eine sehr hohe Zahnzahl enthalten (bis 56). Außer beim 4. Prämolaren bricht nur eine Zahngeneration durch. Enddarm und Vaginalöffnungen münden in eine von einem Ringmuskel umgebene Kloakentasche, ebenso die Harnröhre, sofern sie nicht bei männlichen Tieren an der Basis des Penis mündet. Der ausschließlich samenführende Penis liegt in einer Penistasche und zwar, anders als bei den Höheren Säugetieren, nicht vor, sondern hinter dem Scrotum. Der weibliche Geschlechtsapparat ist mit unterschiedlichem Verwachsungsgrad paarig ausgebildet. Außer bei den Beuteldachsen wird keine Plazenta ausgebildet, die bis zu 11 Embryos werden von Ausscheidungen der Gebärmutterschleimhaut ernährt. Die Brutbeutel der Weibchen sind je nach Art sehr unterschiedlich. Die Zitzen sind sehr lang, damit sich die Neubegorenen an ihnen festsaugen können, vielfach kommt es zu einer sekundären Verwachsung von Jungem und Zitze. Die Jungen verlassen nach einer kurzen Tragzeit von 8-42 Tagen die Gebärmutter und werden danach im Brutbeutel untergebracht, den sie erst nach einer längeren Beuteltragzeit von bis zu 250 Tagen verlassen [1; 5]. VerbreitungSüdamerika und von dort Ausbreitung einiger Arten nach Mittel- und Nordamerika; Australien, Neuguinea, Indonesien östlich der Wallace-Linie, Salomonen. Haltung im ZooIn europäischen Zoos sind die Beuteltiere mit rund 25 Arten schwach vertreten. Das hängt damit zusammen, dass einerseits die Ausfuhr aus Australien sehr restriktiv geregelt ist, andererseits viele Arten klein und nachtaktiv sind und somit dem Publikum in Zoos nur präsentiert werden können, wenn diese über ein Nachttierhaus verfügen. Etwa die Hälfte der gezeigten Arten sind Kängurus (Macropodidae), die andere Hälfte verteilt sich auf 9 Familien. Die in Europa mit Abstand häufigste Art ist das Bennettkänguru (Macropus rufogriseus), das in rund 540 Zoos gezeigt wird, mit Abstand gefolgt vom Roten Riesenkänguru (Macropus rufus) und dem Parmakänguru (Macropus parma) mit jeweils gegen 90 Haltungen [6]. Taxonomie und NomenklaturBeuteltiere waren im Erdmittelalter und in der frühen Erdneuzeit in Nordamerika, Eurasien, Mittel- und Südamerika, der Antarktis und Afrika weit verbreitet, wurden aber bis auf die Beutelratten und Beutelmäuse in Nord- Mittel und Südamerika überall von den Höheen Säugetieren verdrängt oder wurden Opfer des Klimawandels. Nach Australien, wo wir heute die größte Artenvielfalt haben, gelangten sie, von Südamerika her, erst im Eozän, d. h. vor rund 50 Millionen Jahren [1]. Die Beutelsäuger werden als Unterklasse den Ursäugern und Höheren Säugetieren gegenüber gestellt. Früher wurden alle Beuteltiere in einer einzigen Ordnung zusammengefasst [1; 3]. HALTENORTH unterteilte 1969 die Unterklasse in mehrere Ordnungen, was in Analogie zu den Verhältnissen bei den Höheren Säugetieren durchaus gerechtfertigt ist und bis heute Bestand hat [4; 5]. |
Literatur und Internetquellen
- GRZIMEK, B. (1970). In GRZIMEKs TIERLEBEN
- IUCN Red List of Threatened Species. Version 2022-2. Downloaded on 6 January 2023.
- SIMPSON, G. G. (1945)
- WILSON, D. E. et al. eds. (2009-2019)
- ZISWILER, V. (1976)
- ZOOTIERLISTE
Zurück zu Übersicht Kloaken- und Beuteltiere
Weiter zu Nordopossum (Didelphis virginiana)
WADDELL, P. J., OKADA, N. & HASEGAWA, M. (1999)
Towards Resolving the Interordinal Relationships of Placental Mammals.
Systematic Biology 48 (1): 1–5.
DOI: 10.1093/sysbio/48.1.1
Einleitung:
Here we show that progress towards a reliable phylogeny for placental mammals at the ordinal level continues apace. We draw especially upon insights from the recent “International Symposium on the Origin of Mammalian Orders” held at The Graduate University of Advanced Study, Hayama, Japan (21–25 July 1998), particularly work not incorporated in the remainder of this issue or published elsewhere. Abstracts to talks and posters presented at this meeting can be found at www.utexas.edu/ftp/depts/systbiol/ . The talks fell into three main sections, which we will now consider, followed by a summary where we present our current best estimate of the tree for placental mammals.
WADDELL, P. J., KISHINO, H. & OTA, R. (2001)
A Phylogenetic Foundation for Comparative Mammalian Genomics.
Genome Informatics 12: 141–154.
Abstract:
A major effort is being undertaken to sequence an array of mammalian genomes. Coincidentally, the evolutionary relationships of the 18 presently recognized orders of placental mammals are only just being resolved. In this work we construct and analyse the largest alignments of amino acid sequence data to date. Our findings allow us to set up a series of superordinal groups (clades) to act as prior hypotheses for further testing. Important findings include strong evidence for a clade of Euarchonta+ Glires (=Supraprimates) comprised of primates, flying lemurs, tree shrews, lagomorphs and rodents. In addition, there is good evidence for a clade of all placental mammals except Xenarthra and Afrotheria (=Boreotheria) and for the previously recognised clades Laurasiatheria, Scrotifera, Fereuungulata, Ferae, Afrotheria, Euarchonta, Glires, and Eulipotyphla. Accordingly, a revised classification of the placental mammals is put forward. Using this and molecular divergence-time methods, the ages of the superordinal splits are estimated. While results are strongly consistent with the earliest superordinal divergences all being > 65 mybp (Cretaceous period), they suffer from greater uncertainty than presently appreciated. The early primate split of tarsiers from the anthropoid lineage at ∼55 mybp is seen to be an especially informative fossil calibration point. A statistical framework for testing clades using SINE data is presented and reveals significant support for the tarsier/anthropoid clade, as well as the clades Cetruminantia and Whippomorpha. Results also underline our thesis that while sequence analysis can help set up hypothesised clades, SINEs obtainable from sequencing 1-2 MB regions of placental genomes are essential to testing them. In contrast, derivations suggest that empirical Bayesian methods for sequence data may not be robust estimators of clades. Our findings, including the study of genes such as TP53, make a good case for the tree shrew as a closer relative of primates than rodents, while also showing a slower rate of evolution in key cell cycle genes. Tree shrews are consequently high value experimental animals and a strong candidate for a genome sequencing initiative.
SIMPSON, G. G. (1945)
The principles of classification and a classification of mammals.
Bulletin of the American Museum of Natural History 85.
16+350 Seiten.
George Gaylord SIMPSON war Kurator für fossile Säugetiere und Vögel am Amerikanischen Museum für Naturkunde in New York. Die von ihm begründete Klassifizierung der Säugetiere hatte ein halbes Jahrhundert Bestand und wurde während dieser Zeit im Wesentlichen von den säugetierkundlichen Standardwerken übernommen. Im deutschsprachigen Raum wurde diese Systematik vor allem durch eine Veröffentlichung von MÜLLER-USING und HALTENORTH aus dem Jahr 1954, die in den „Säugetierkundlichen Mitteilungen" auf der Basis der SIMPSON’schen Klassifikation für die rezenten 22 Unter- und 10 Teilordnungen sowie für die 52 Überfamilien und 118 Familien der Säugetiere deutsche Namen vorschlugen.
simpson-biblio
O'LEARY, M. A., BLOCH, J. I. et al. (2013)
O'LEARY, M. A., BLOCH, J. I., FLYNN, J. J., GAUDIN, T. J., GIALLOMBARDO, A., GIANNINI, N. P., GOLDBERG, S. L., KRAATZ, B. P., LUO, Z.-X., MENG, J., NI, X., NOVACEK, M. J PERINI, F. A., RANDALL, Z. S., ROUGIER, G. W., SARGIS, E. J., SILCOX, M. T., SIMMONS, N. B., SPAULDING, M., VELAZCO, P. M., WEKSLER, M., WIBLE, J. R. & CIRRANELLO, A. L. (2013)
The Placental Mammal Ancestor and the Post–K-Pg Radiation of Placentals.
Science (08 Feb 2013) 339 (6120): 662-667.
DOI: 10.1126/science.1229237
Abstract:
To discover interordinal relationships of living and fossil placental mammals and the time of origin of placentals relative to the Cretaceous-Paleogene (K-Pg) boundary, we scored 4541 phenomic characters de novo for 86 fossil and living species. Combining these data with molecular sequences, we obtained a phylogenetic tree that, when calibrated with fossils, shows that crown clade Placentalia and placental orders originated after the K-Pg boundary. Many nodes discovered using molecular data are upheld, but phenomic signals overturn molecular signals to show Sundatheria (Dermoptera + Scandentia) as the sister taxon of Primates, a close link between Proboscidea (elephants) and Sirenia (sea cows), and the monophyly of echolocating Chiroptera (bats). Our tree suggests that Placentalia first split into Xenarthra and Epitheria; extinct New World species are the oldest members of Afrotheria.