BLOM, A., ALERS, M. P. T., FEISTNER, A. T. C., BARNES, R. F. W & BARNES, K. L. (1992)
Primates in Gabon - current status and distribution
ORYX 26 (4):223-234. ISSN 0030-6053. DOI: http://dx.doi.org/10.1017/S0030605300023759
Abstract:
This paper examines the current status and distribution of primates in Gabon on the basis of data collected in the field between 1985 and 1988. There are at least 19 and possibly 21 species of primates definitely present in Gabon, making it one of the richest countries in the world for primates. Most of the species are still widespread and one, the sun-tailed guenon, is endemic. Hunting and habitat destruction are the main threats to the country's primates. The major problem at the moment is the opening up of previously inaccessible areas by logging companies and the Trans Gabon railway, which leads to an increase in hunting pressure. Several species are threatened; the mandrill/drill, the black colobus, and the sun-tailed guenon need special conservation measures. Suggestions for action are made and several new reserves have recently been proposed.
ANGST, C. (2010)
Mit dem Biber leben: Bestandeszählung 2008.
Perspektiven für den Umgang mit dem Biber in der Schweiz.
156 Seiten, 85 Abbildungen, Tabellen. Bundesamt für Umwelt, Ittigen/Bern & Schweizer Zentrum für die Katographie der Fauna, Neuenburg.
Zusammenfassung:
200 Jahre nach seiner Ausrottung hat sich der Biber in der Schweiz wieder gut etab- liert. Seine Wiederansiedlung zwischen 1956 und 1977 ist eine Erfolgsgeschichte desSchweizer Artenschutzes. Nachdem die Biberpopulation während Jahren nur langsamwuchs, besiedeln heute wieder 1600 Biber unsere Gewässer, wie eine Bestandeserhe-bung im Winter 2007/08 ergab. Aufgrund dieses erfreulichen Resultates kann der Biberbei der geplanten Revision der Roten Liste von der heutigen Klassierung vom Ausster-ben bedroht (critically endangered) auf verletzlich (vulnerable, IUCN)zurückgestuft werden.
Der Biber hat einen grossen Teil der potenziell besiedelbaren Gewässer besetzt. DieBestände entlang der grossen Mittellandflüsse bilden heute die Kerne der SchweizerBiberpopulation. Diese gilt es unbedingt zu erhalten und zu fördern, damit sie nichtwieder abnimmt. Jungbiber haben nämlich immer mehr Mühe, neue, konfliktfreieLebensräume zu finden. Die Fliessgewässerstruktur ist vielfach schlecht, und denGewässern fehlt genügend Raum, damit der Biber ungestört seinen Aktivitäten nach-gehen kann. Mit dem Gegenvorschlag Schutz und Nutzung der Gewässer zur Volksini-tiative «Lebendiges Wasser» (Renaturierungs-Initiative) erhalten die Kantone wirksa-me Instrumente, um diese beiden Forderungen in Zukunft umzusetzen. Damit werden neue, konfliktfreie Lebensräume für den Biber geschaffen. Als wichtige Schlüsselartder Gewässer kann uns der Biber im Gegenzug helfen, die Gewässer in einen natürli-cheren Zustand zurückzuführen. Gleichzeitig fördert er durch seine vielfältigen Aktivi-täten die Biodiversität.
angst-biblio
AUBRECHT, G. (1985)
Der Waschbär, Procyon lotor (LINNÉ, 1758), in Österreich.
(Mammalia Austriaca 11). Jb. Oö. Mus.-Ver. 130: 243-257.
Zusammenfassung:
Aus Bayern kommend, haben Waschbären 1974 erstmals Österreich erreicht. Bis 1984 stammen Beobachtungen aus den Bundesländern Vorarlberg, Salzburg, Oberösterreich, Niederösterreich und Wien. Die Ausbreitungsgeschichte, Taxonomie, Biologie und Ökologie dieser faunenfremden Art werden
diskutiert.
aubrecht-biblio
BEZZEL, E. (1994)
Situation und Bestand des Steinadlers (Aquila chrysaetos) in Deutschland.
Journal of Ornithology 135: 113-115.
Abstract:
The present population of Golden Eagles in Germany consists of 48–50 territorial pairs in the Alps (10 % of them with homeranges extending beyond the border to Austria) and a considerable amount of nonterritorial individuals (mostly immat.). As the production is very low (0.25 resp. 0.18 fledglings/pair x year) nonterritorial birds form an important breeding reserve. At least within last decades, the abundance seemed to be fairly constant. At present, the German population depends on immigration from other parts of the alpine population.
bezzel-biblio
04.03.2013 - 1'032
BARTEL, M., GRAUER, A., GREISER, G., HEYEN, B., KLEIN, R., MUCHIN, A., STRAUSS, E., WENZELIDES, L. & WINTER, A. (2007)
Wildtier-Informationssystem der Länder Deutschlands.
Status und Entwicklung ausgewählter Wildtierarten in Deutschland, Jahresbericht 2006.
Deutscher Jagdschutz- Verband e.V. (Hrsg.). VII + 98 Seiten, zahlreiche Abbildungen. ISSN 1863 - 7582
Zusammenfassung:
Mit dem Wildtier-Informationssystem der Länder Deutschlands (WILD) wurde erstmals ein bundesweites Monitoring-Programm zur großflächigen Populationserfassung bejagbarer Wildtiere installiert.
Der Deutsche Jagdschutz-Verband gab das Projekt als dauerhaften Baustein der ökologischen Umweltbeobachtung mit dem Ziel in Auftrag, Strategien für Schutz und nachhaltige Nutzung von Tierpopulationen zu entwickeln. Die Erfassung von Populationsdichten und -entwicklungen dient als Basis für weitere Forschung und als Argumentationsbasis für jagdpolitische und naturschutzrelevante Entscheidungen in Deutschland. Die Daten des Monitoring-Programms „Greifvögel und Eulen Europas“ fließen durch Unterstützung der Game Conservancy Deutschland e.V. und des DJV mitin das WILD ein und ergänzen es um einen weiteren Baustein.
Die Datenerhebung in WILD basiert zum einen auf Wildtierzählungen in ausgewählten Referenzgebieten, zum anderen auf Bestandseinschätzungen in möglichst vielen Jagdbezirken Deutschlands. In dem langfristig angelegten Projekt werden auch Faktoren, die Einfluss auf die Dichte der untersuchten Tierarten nehmen können (z.B. Flächennutzung, Jagdintensität, differenzierte Jagdstrecken), erhoben.
bartel-biblio
TOBLER, U. (2011)
Differential responses on individual- and population-level to a fungal pathogen: Bd infection in the midwife toad Alytes obstetricans.
125 Seiten.
2011 PhD Thesis, University of Zurich, Faculty of Science.
Volltext
Zusammenfassung
Infektionskrankheiten werden zu einer immer stärkeren Bedrohung der Biodiversität, und die Anzahl bekannter Wildtierkrankheiten, die sich ausbreiten, nimmt dramatisch zu (Daszak et al. 2000, Smith et al. 2009). Die Problematik kommt daher, dass Krankheitserreger, die ein breites Wirtsspektrum haben, in naive Populationen eingeschleppt werden, zusammen mit ihren relativ resistenten ursprünglichen Wirten, die als Überträger dienen (Daszak et al. 2004).
Gemäss der IUCN sind Amphibien die am stärksten bedrohte Wirbeltiergruppe; rund ein Drittel der Arten ist bedroht (Gascon et al. 2007). Eine Pilzerkrankung, die Chytridiomykose, wurde als eine wichtige Ursache der Bestandesrückgänge identifiziert. Deren Erreger, der Pilz Batrachochytrium dendrobatidis (Bd) ist ein Chytridiomycet, der die keratinisierte Haut von Amphibien befällt und mit dem lokalen und globalen Aussterben von Amphibien auf mehreren Kontinenten in Verbindung gebracht wird (Fisher et al. 2009b, Kilpatrick et al. 2010). Bd wird hauptsächlich im Wasser übertragen und ein langes Kaulquappenstadium, wie es bei der Geburtshelferkröte vorkommt, erhöht somit das Ansteckungsrisiko. Infektionen bei Kaulquappen sind auf die Mundfelder beschränkt, was keine Krankheitssymptome bewirkt. Im Gegensatz dazu sind die Tiere kurz nach der Metamorphose am anfälligsten, wenn die gesamte Amphibienhaut von Keratin überzogen wird und das Immunsystem erst schwach ausgebildet ist (Rollins-Smith 1998). Nebst Unterschieden in der Krankheitsanfälligkeit verschiedener Lebensstadien beobachtet man auch Unterschiede aufgrund von Hautpeptiden, der Lebensweise und dem Verhalten; auch bakterielle Symbionten auf der Amphibienhaut und klimatische Bedingungen dürften eine Rolle spielen (Fisher et al. 2009b, Kilpatrick et al. 2010). So sind manche Arten relativ resistent und erkranken nicht, während bei anderen Arten Massensterben auftreten. Geburtshelferkröten-Populationen in einem Nationalpark in Spanien nahe Madrid nahmen beispielsweise drastisch ab, nachdem Bd dort erstmals nachgewiesen wurde (Bosch et al.2007, Bosch et al. 2001); daher ist die Annahme begründet, dass Bd auch in anderen Verbreitungsgebieten der Art zu Bestandesabnahmen führt.
In der Schweiz hat die Geburtshelferkröte in den letzten drei Jahrzehnten massive Bestandesrückgänge erlitten (Schmidt & Zumbach 2005). Vielen lokalen Aussterbeereignissen kann keine offensichtliche Ursache zugewiesen werden und daher ist eine eher kryptische Ursache wie eine Infektionskrankheit eine plausible alternative Erklärung.
Im ersten Kapitel meiner Dissertation bestimme ich den geographischen Massstab, in dem Geburtshelferkröten-Populationen organisiert sind. Die meisten Arten sind in Populationen organisiert, die ihrerseits Netzwerke aus Subpopulationen sind. Diese Netzwerke zeichnen sich durch einen unterschiedlichen Grad an Genfluss zwischen einzelnen Subpopulationen aus (Wright 1965). In meiner Arbeit untersuchte ich die genetische Struktur von Geburtshelferkröten in vier Regionen der Schweiz. Alle vier Regionen beherbergen Netzwerke von Subpopulationen, die sich in der Stärke der Bestandesabnahmen, im Grad ihrer Vernetzung und einer Reihe weiterer Ursachen, die die genetische Struktur beeinflussen können, unterscheiden. Anhand neutraler Mikrosatellitenmarker bestimmte ich die genetische Diversität und Differenzierung innerhalb der Regionen. Mittels Modellselektion suchte ich die Faktoren, die die Unterschiede in der genetischen Struktur zwischen den Regionen am besten erklären. Wir fanden keine Hinweise darauf, dass die Stärke der Bestandesabnahmen mit der genetischen Diversität korreliert. Ebenso wenig war die genetische Differenzierung mit der Isolation der Subpopulationen korreliert; alle Populationen waren genetisch isoliert, selbst über geringe Distanzen. Nur die Höhenlage hatte einen Einfluss auf die genetische Diversität: Sie nahm mit zunehmender Höhenlage zu. Fluktuierende Umweltbedingungen in grösseren Höhenlagen sind eine mögliche Erklärung für diese Beobachtung (Fisher 1930, Munwes et al. 2010). Das Fehlen eines Zusammenhangs zwischen Bestandesrückgängen und genetischer Zusammensetzung deutet darauf hin, dass Geburtshelferkröten-Subpopulationen als relative unabhängige Einheiten funktionieren und Genfluss zwischen Subpopulationen relativ unwichtig ist (Beebee 2005, Frankham et al. 2002). Daher sollten sich Auswirkungen der Infektionskrankheit anhand ihres Effekts auf einzelne Populationen zeigen lassen, unabhängig vom Infektionsstatus benachbarter Populationen.
In Kapitel 2 quantifiziere ich die Mortalität von mit Bd infizierten Geburtshelferkröten nach der Metamorphose. Dazu fing ich natürlicherweise infizierte Kaulquappen von drei verschiedenen Populationen und zog sie im Labor auf. Die Kaulquappen wurden in drei Behandlungsgruppen eingeteilt: 1) Die Bd-negative Kontrolle befreite ich durch die Behandlung mit dem fungiziden Medikament Itraconazol von der Infektion (Garner et al.2009a). 2) Die Stresskontroll-Gruppe behandelte ich nach dem gleichen Protokoll wie die Bd-negative Kontrolle, verzichtete aber auf das Itraconazol während der Behandlung. Diese Gruppe erfuhr also denselben Behandlungsstress wie die Itraconazol-behandelte Gruppe, blieb aber infiziert. 3) Die letzte Gruppe wurde nicht behandelt und nur die regulären Wasserwechsel und Fütterungen, die bei allen Versuchsgruppen stattfanden, wurden vorgenommen. Auch diese Gruppe blieb demnach infiziert. Die Resultate zeigen, dass die Mortalität durch Bd-Infektion hoch war (44.4% aller infizierten Tiere starben), aber dass es grosse Unterschiede zwischen den verschiedenen Populationen gab (die Sterblichkeit schwankte zwischen 27% und 90%). Die Unterschiede, die wir beobachteten, könnten auf unterschiedliche symbiotische Hautbakterien, unterschiedliche Erregerstämme oder Umwelteffekte vor dem Fang im natürlichen Lebensraum zurückzuführen sein. Umwelteffekte lassen jedoch über kurze Zeit nach (Van Buskirk 2002) und Hautbakterien und Erregerstämme wurden aufgrund unseres Laborprotokolls zwischen den Populationen vermutlich vermischt. Daher gehen wir davon aus, dass genetische Unterschiede zwischen den Populationen die Unterschiede in der Mortalität bewirkt haben.
Wie die hohe Sterblichkeit, die wir im 2. Kapitel beobachteten, zeigt, sind Auswirkungen von Bd auf die Überlebenswahrscheinlichkeit der Populationen anzunehmen. Daher versuche ich im 3. Kapitel einen Zusammenhang zwischen dem Vorkommen von Bd in einer Population und dem lokalen Aussterben der Geburtshelferkröte herzustellen. Dazu benützten wir Daten aus der Erhebung, die im Rahmen der Aktualisierung der Roten Liste in 2003 und 2004 durchgeführt wurde (Schmidt & Zumbach 2005). Anhand dieser Daten wählten wir 79 Teiche, verteilt über das gesamte Verbreitungsgebiet der Geburtshelferkröte in der Schweiz, von denen wir wussten, dass sie um ca. 1985 Geburtshelferkröten-Populationen beherbergt hatten. Wir besuchten diese Teiche in 2008 und testeten sie auf das Vorkommen von Bd, indem wir Hautabstriche von Amphibien sammelten, die wir an den Teichen fingen. Diese Abstriche wurden im Labor mittels real-time PCR auf Bd getestet (Boyle et al. 2004). Gleichzeitig führten wir eine erneute Erhebung über die Anwesenheit von Geburtshelferkröten an den Teichen durch. Die Anwesenheit von Bd und Geburtshelferkröten wurden dann in einem hierarchischen Modell analysiert, das die Vorkommenswahrscheinlichkeit mehrerer Arten während mehrerer Erhebungsperioden modelliert. Bei dieser Art von Modellen wird die Antreffwahrscheinlichkeit einer Art mitberücksichtigt. Ich modellierte also gleichzeitig die Vorkommenswahrscheinlichkeit von Bd in 2008 und die Vorkommenswahrscheinlichkeit der Geburtshelferkröte während den zwei Erhebungen in 2003/2004 und 2008 in einem einzigen Modell. Dieses Modell berechnete ich in mit dem Programm WinBUGS (Kéry 2010, Royle & Dorazio 2008), das auf dem Bayes’schen Theorem bedingter Wahrscheinlichkeiten beruht. Dadurch war es mir möglich, die Wahrscheinlichkeit, dass die Geburtshelferkröte vorkommt, ausgestorben ist oder überlebt hat an einem Teich, und die Wahrscheinlichkeit, dass Bd vorkommt, in Abhängigkeit von einander modellieren und dabei jeweils den Fehler der geschätzten Wahrscheinlichkeiten berücksichtigen (Waddle et al. 2010). Dabei zeigte sich, dass das Vorkommen bzw. die lokale Aussterbewahrscheinlichkeit der Geburtshelferkröte unabhängig vom Vorkommen von Bd ist. Dieses überraschende Ergebnis wird durch die Resultate aus meinem nächsten Kapitel gestützt.
Im 4. Kapitel untersuche ich die Wachstumsraten von Geburtshelferpopulationen in An- oder Abwesenheit von Bd. Adrian Borgula stellte grosszügigerweise die jährlichen Ruferzählungen von 26 Teichen im Kanton Luzern von 2002 bis 2009 zur Verfügung. Für jede Population modellierte ich den Populationstrend in Abhängigkeit des Vorkommens von Bd und der Häufigkeit nachgewiesener Fortpflanzung. Dieses Modell wurde wiederum im Programm WinBUGS beruhend auf dem Bayes’schen Wahrscheinlichkeitstheorem berechnet. Der Vorteil dieses Ansatzes gegenüber konventionellen Maximum-Likelihood Schätzung ist, dass bei der Analyse der Fehler im Populationstrend, der durch den Beobachtungsprozess und den Prozess der Analyse entsteht, berücksichtigt wird. Wiederum fanden wir keinen negativen Zusammenhang zwischen dem Vorkommen von Bd und den Wachstumsraten der Geburtshelferkröten-Populationen. Das Fehlen eines Zusammenhangs zwischen dem Vorkommen von Bd und lokalen Bestandesabnahmen (Kapitel 4) oder lokalem Aussterben (Kapitel 3) der Geburtshelferkröte kann durch mehrere Mechanismen zustande kommen, die einander nicht zwingend ausschliessen: 1) Möglicherweise begünstigen die herrschenden Umweltbedingungen keine Krankheitsausbrüche (Bosch et al.2007, Rohr et al. 2008, Walker et al. 2010). 2) Andererseits kann Bd sowohl als enzootische als auch als epizootische Infektion vorliegen (Briggs et al. 2010). Während epizootische Krankheitsdynamik meist additive, d.h. zusätzliche, Mortalität bewirkt, besteht bei enzootischer Dynamik die Möglichkeit, dass die Mortalität kompensiert wird. Bd in der Schweiz könnte mehrheitlich enzootische Krankheitsdynamik bewirken. 3) Bd verringert möglicherweise nicht die Überlebenswahrscheinlichkeit, sondern wirkt sich auf andere Fitnessparameter von Individuen aus. Ist das Leistungsvermögen in einem Fitnessbereich reduziert, kann möglicherweise eine gesteigerte Effizienz in anderen Fitnessbereichen für die Verluste kompensieren (Jolles et al. 2005). 4) Möglich ist auch, dass Bd zu Beginn nach dem ersten Auftreten eine Bestandesabnahme bewirkt hat und dass sich die Populationen jetzt auf einem geringeren Niveau stabilisiert haben (Briggs et al. 2005). Die Prävalenz und Abundanz von Bd variiert stark zwischen verschiedenen Populationen. Massensterben treten nur auf, wenn die Abundanz von Bd sehr hoch ist (Briggs et al. 2010, Vredenburg et al. 2010).
Daher versuche ich in Kapitel 5 diese Unterschiede durch die Umwelteigenschaften der Gewässer zu erklären. Dazu wählte ich 19 Teiche in den drei Gebieten, die ich in Kapitel 1 bereits beprobt hatte und in denen Bdvorkam, nämlich BE, BL und SG. An diesen 19 Teichen beprobte ich im Frühling und Sommer Kaulquappen der Geburtshelferkröte auf Bd und mass von April bis Oktober Umweltdaten. Anhand eines hierarchischen Bayes-Modells schätzte ich die Auswirkungen der Amphibiendichte, der Wassertemperatur, der genetischen Diversität der Wirtspopulation und der Zooplanktondichte auf die Entdeckungs- und Vorkommenswahrscheinlichkeit und Abundanz des Erregers ab. Da Abundanzmodelle eine grosse Anzahl an Iterationen benötigen, bis sie konvergieren, sind die Ergebnisse, die in diesem Kapitel präsentiert werden, erst vorläufig und ändern möglicherweise noch, bis ein Modell gefunden ist, das optimal konvergiert. Die Effekte der Kovariaten Amphibiendichte, Wassertemperatur und Zooplanktondichte sollten qualitativ robust sein, auch wenn die Schätzwerte noch ändern können. Bd war häufiger in wärmeren Teichen, vermutlich weil sogar warme Gewässer in unseren Breitengraden sich nie für längere Zeit über das Wachstumsoptimum von Bd hinaus erhitzen. Eine höhere Kaulquappendichte korrelierte mit einer höheren Abundanz von Bd. Die Ergebnisse belegen, dass Umwelteigenschaften einen Einfluss auf die Abundanz von Bdhaben. Dieses Wissen könnte wichtig werden, wenn es darum geht, Habitatmanagement zu betreiben, um die Auswirkungen von Bd zu reduzieren. Während meiner Dissertation gelang es mir zu zeigen, das Bd auf Individuenebene ein ernst zu nehmender Krankheitserreger sein kann und hohe Mortalität bewirkt. Auf Populationsebene jedoch beobachten wir keine negativen Auswirkungen von Bd. Entweder können die Verluste kompensiert werden oder die Mortalität ist gering, da die Umweltbedingungen keine Krankheitsausbrüche begünstigen. Da die Abundanz des Erregers von den Umweltbedingungen abhängt, kann die Manipulation des Lebensraums der Geburtshelferkröte eine sinnvolle Massnahme zur Verringerung der Auswirkungen von Bd in Zukunft darstellen.
tobler-biblio
STIRLING, I. (2002)
Polar Bears and Seals in the Eastern Beaufort Sea and Amundsen Gulf:
A Synthesis of Population Trends and Ecological Relationships over Three Decades.
ARCTIC, Vol. 55, SUPP. 1: 59-76.
Abstract:
In the eastern Beaufort Sea and Amundsen Gulf, research on polar bear populations and their ecological interrelationships with seals and sea ice conditions began in the fall of 1970. Analysis of movement data from mark-recapture studies and tracking of adult female bears with satellite radio collars indicated that there are two populations of polar bears in the area, one that inhabits the west coast of Banks Island and Amundsen Gulf and a second that is resident along the mainland coast from about Baillie Islands in Canada to approximately Icy Cape in Alaska. Polar bears throughout the Beaufort Sea and Amundsen Gulf were severely overharvested before the establishment of quotas in Canada in 1968 and the cessation of all but subsistence polar bear hunting in Alaska in 1972. Since then, both populations have recovered, and the population estimates currently used for management purposes are 1200 and 1800 for the Northern and Southern Beaufort populations, respectively. However, these population estimates are now dated and should be redone. Most female polar bears in the Beaufort Sea breed for the first time at 5 years of age, compared to 4 years of age in most other populations, and cubs normally remain with their mothers for 2.5 years prior to weaning. Heavy ice conditions in the mid-1970s and mid-1980s caused significant declines in productivity of ringed seals, each of which lasted about 3 years and caused similar declines in the natality of polar bears and survival of subadults, after which reproductive success and survival of both species increased again. The changes in the sea ice environment, and their consequent effects on polar bears, are demonstrable in parallel fluctuations in the mean ages of polar bears killed each year by Inuit hunters. In 1989, the decadal-scale pattern in fluctuations of ice conditions in the eastern Beaufort Sea changed in response to oceanographic and climatic factors, and this change has resulted in greater amounts of open water in recent years. In addition, climatic warming will be a major environmental factor if greenhouse gas emissions continue to increase. It is unknown whether the ecosystem will return to the pattern of decadal-scale change exhibited in previous decades, or how polar bears and seals will respond to ecological changes in the future, but research on these topics is a high priority.
stirling-biblio
ALMASAN, H. (1994)
Die Entwicklung der Bärenpopulation in Rumänien.
Wildbiologie International 5/10. Wildtier Schweiz, Zürich.
Auszug:
Rumänien – für Kenner ein Land der Bären. Im Gegensatz zu den wenigen Restpopulationen Westeuropas leben dort die Bären, besonders in den wilden Karpaten, in einem vitalen Bestand.
Nach dem Fall der Diktatur dürfen Rumänen und ausländische Gäste wieder auf die Jagd – auch auf den Bären. Die Sorge rumänischer Wildtierbiologen gilt nun einem Management nach wildtiergerechten Kriterien. Eine Bejagung der Bären soll möglich sein, vor allem aber muss die Populationsstruktur erhalten bleiben.
almasan-biblio
Japanischer Serau
Überordnung: LAURASIATHERIA
Taxon ohne Rang: CETARTIODACTYLA
Ordnung: Paarzeher (ARTIODACTYLA)
Unterordnung: Wiederkäuer (Ruminantia)
Familie: Hornträger (Bovidae)
Unterfamilie: Ziegenartige: (Caprinae)
Tribus: Gemsenverwandte (Naemorhedini)
Japanischer Serau
Capricornis crispus • The Japanese Serow • Le saro du Japon
- Körperbau und Körperfunktionen
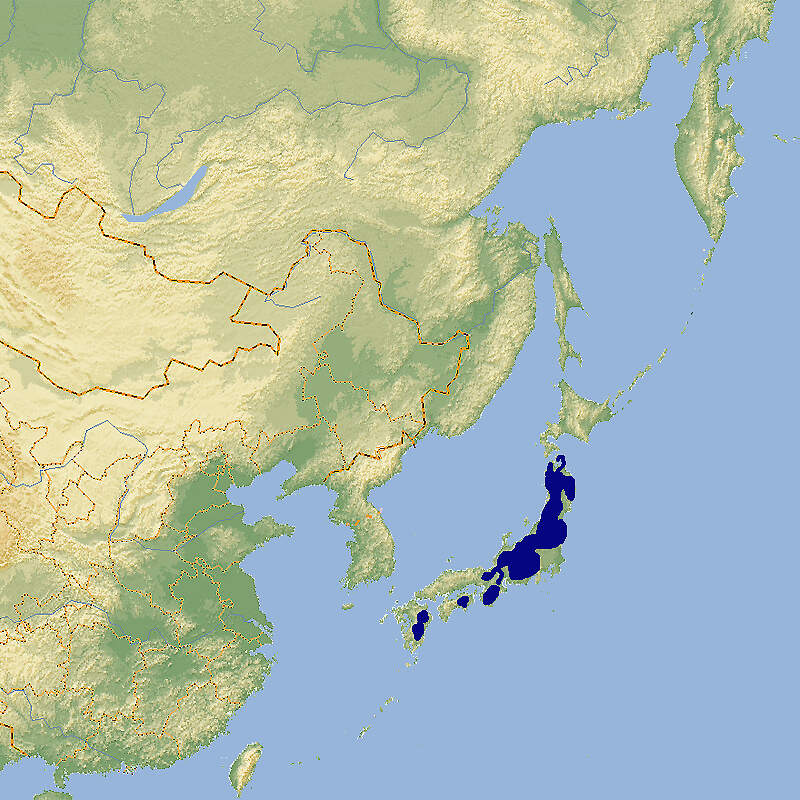
- Verbreitung
- Lebensraum und Lebensweise
- Gefährdung und Schutz
- Bedeutung für den Menschen
- Haltung
- Taxonomie und Nomenklatur
- Literatur und Internetquellen
|
Weitere Bilder auf BioLib.cz |
Der Japanische Serau ist ein in seiner Heimat nicht gefährdeter Gemsenverwandter, der in Japan in vielen Zoos gezeigt wird, in Europa aber stets nur selten zu sehen war und gegenwärtig (2019) nicht mehr gehalten wird. Ein Grund für die geringe Beliebtheit der Art dürfte ihre einzelgängerische Lebensweise und ihre hohe innerartliche Aggression sein. Körperbau und KörperfunktionenBeim Japan-Serau gibt es praktisch keinen Geschlechtsdimorphismus. Die Tiere erreichen eine Kopf-Rumpflänge von etwa 130 cm, eine Schulterhöhe von 68-80 cm und ein Gewicht von 31-48 kg. Die leicht gekrümmten Hörner werden 12-16 cm lang. Der Schwanz ist mit 6-8 cm sehr kurz. Stark ausgeprägte Voraugendrüsen finden sich bei beiden Geschlechtern, ebenso Zwischenzehendrüsen. Das Fell ist lang und dicht. Seine Grundfärbung ist blaugrau oder graubraun mit weißen Haaren gesprenkelt, stellenweise schwarz. Die Beine, Ohren und der nackte Nasenspiegel und der kaum behaarte Nasenrücken sind schwarz, allenfalls dunkelbraun, die Kehle und Backenbärte weiß oder hellgrau [1; 6; 8; 13]. VerbreitungJapan: Honshu, Shikoku, Kyushu. In den letzten 30 Jahren konnte der Serau sein Verbreitungsgebiet von rund 34'500 km² auf gegen 60'000 km² ausweiten [5]. Lebensraum und Lebensweise Der Japan-Serau besiedelt alpine Rasen, subalpine Koniferenwälder und Laubwälder der kollinen Stufe [5]. Die Tiere sind hauptsächlich tagsüber aktiv, können aber auch nachts weiden.Sie sind gewöhnlich Einzelgänger, gelegentlich werden aber auch Gruppen bis zu 7 Tieren angetroffen. Die Einzeltiere haben Streifgebiete von wenigen Hektar, die sie als Territorium mit dem wachsartigen Sekret ihrer Voraugendrüsen und durch feste Kotplätze markieren und gegen Artgenossen verteidigen. Oft stehen sie reglos an einer exponierten Stelle, um Präsenz zu markieren. Familienterritorien können bis etwa 22 ha groß sein. Seraue nutzen ein weites Spektrum an Nahrungspflanzen einschließlich Koniferen. Bevorzugt fressen sie Laub von immergrünen und winterkahlen Bäumen und Sträuchern, ferner Farne sowie Gräser, Kräuter und Früchte [2; 5; 7]. Im Gegensatz zu den tropischen Serau-Arten haben die Japan-Seraue eine feste Paarungszeit, die von September bis November dauert. Nach einer Tragzeit von 195-210 Tagen wird im Mai-Juli meistens ein einzelnes Kitz gesetzt, seltener Zwillinge. Seraukitze wiegen bei der Geburt 2,9 bis 3,5 kg. Sie können 12 bis 20 (selten 30) Minuten nach der Geburt gehen und folgen ihrer Mutter. Sie nehmen ab dem 6.- 16. Lebenstag feste Nahrung auf und sind vor der nächsten Brunst der Geiß entwöhnt. Die Geschlechtsreife wird mit anderthalb Jahren erreicht [2; 3]. Gefährdung und SchutzIn der ersten Hälfte des 20. Jahrhunderts büßte der Japanische Serau große Teile seines Areals ein. Heute ist er weit verbreitet, hat eine große Gesamtpopulation (ca. 100'000 Tiere) und stabile bis zunehmende Bestände. Sein Areal ist mittlerweileetwa anderthalb mal so groß wie die Schweiz. Er wurde deshalb im Rahmen einer Beurteilung im Jahr 2008, bestätigt 2020, als nicht-gefährdet eingestuft (Rote Liste: LEAST CONCERN) [5]. Der internationale Handel ist nicht nach CITES geregelt. Bedeutung für den MenschenDer Serau wurde in Japan traditionell zur Fleischgewinnung gejagt. Bis in die 195034-Jahre war dies nicht nachhaltig und meistens illegal. Nachdem die Wilderer-Syndikate eliminiert werden konnten, nahmen die Bestände zu, mit dem Ergebnis, dass es zu größeren forstwirtschaftlichen Schäden kam, was die Behörden veranlasste die Bestände zu reduzieren [5]. HaltungBei der Gehegegestaltung ist zu berücksichtigen, dass Seraue wenig sozial sind. Abtrenngehege und Einzelboxen sind daher Pflicht. Gehege für kleine Gruppen sollten größer sein, als in den Mindestanforderungen vorgegeben und sollten über Sichtblenden und Rückzugsmöglichkeiten verfügen. WEIGL gibt als Höchstalter im Zoo 24 Jahre an, erreicht von einer zoogeborenen Geiß in einem japanischen Zoo, andernorts wird auf ein Rekordalter von 27 Jahren, 7 Monaten und 25 Tagen verwiesen [2; 6]. Die Welterstzucht gelang am 25. August 1965 im Kobe Oji-Zoo von einem Paar, das 1964 gefangen worden war [9]. Für den Japanischen Serau gibt es seit 1971 ein Internationales Zuchtbuch, das früher am Tiergarten Schönbrunn geführt wurde und heute am Toyama Familienpark-Zoo in Japan geführt wird. Dieses umfasste im Dezember 2016 796 lebende Individuen in 130 Einrichtungen [IZY 52]. Haltung in europäischen Zoos: Die Ersteinfuhr nach Europa erfolgte 1879 durch den Londoner Zoo. Währenddem die Art in japanischen Zoos häufig anzutreffen ist, war sie außerhalb ihres Ursprungslands stets selten. 2007 wurde mit 45 Individuen in europäischen und nordamerikanischen Zoos der Höchststand erreicht, danach erfolgte ein dramatischer Rückgang bis 2014 auf noch 22 Tiere [1], und seitdem ist der europäische Bestand ganz ausgestorben. Bis 2018 lebte in Aussig an der Elbe noch ein einzelnes Tier. Dem nordamerikanischen Bestand, der 2019 noch 10 Tiere in 4 Haltungen umfasste, droht dasselbe [10]. Für Details siehe Zootierliste. Im Tiergarten Schönbrunn war 1994 die europäische Erstzucht gelungen, dem Zoologischen Garten Berlin 1997 die deutsche Erstzucht. Mindestanforderungen an Gehege: Nach Säugetiergutachten 2014 des BMEL soll für bis zu 5 Tieren ein Gehege von mindestens 250 m² zur Verfügung stehen, für jedes weitere Tier 20 m² zusätzlich. Ein Stall ist nicht erforderlich. Die Schweizerische Tierschutzverordnung (Stand 01.06.2022) schreibt für bis zu 4 Tieren ein Gehege vor, dessen Grundfläche 500 m² misst. Für jedes weitere Tier kommen 50 m² zur Basisflächen dazu. Es sind natürliche oder künstliche Unterstände anzubieten, in denen alle Tiere gleichzeitig Platz finden. Werden die Tiere aufgestallt, ist eine Grundfläche von mindestens 4 m²/Tier vorgeschrieben. Nach der 2. Tierhaltungsverordnung Österreichs (Stand 2023) sind für bis zu 10 Tiere 500 m² erforderlich, für jedes weitere 50 m² mehr. Es müssen Unterstände zum Schutz gegen Witterungsverhältnisse wie Regen, Wind, Sonneneinstrahlung und Hitze angeboten werden, so dass alle Tiere bei Bedarf darin gleichzeitig Unterschlupf finden können. Die Haltung hat in Herden zu erfolgen. Taxonomie und NomenklaturDer Japanische Serau wurde 1844 von Coenraad Jacob TEMMINCK vom Naturhistorischen Museum in Leiden als "Antilope crispa" erstmals wissenschaftlich beschrieben. Die gegenwärtig gültige Gattung Capricornis wurde 1836 von dem aus Irland stammenden Naturforscher William OGILBY aufgestellt [7; 8]. Die Systematik der Seraue ist nicht ganz klar, Die Caprinae Spezialisten-Gruppe der IUCN geht von 3, WILSON & REEDER sowie die Rote Liste der IUCN gehen von sechs Arten aus. Das Handbook of the Mammals of the World von 7. Von den Goralen werden vier Arten unterschieden. Bisweilen werden Seraue und Gorale in einer Gattung (Naemorhedus) zusammengefasst [4; 5; 7; 8]. |
Literatur und Internetquellen
- HOLLAND, J. & PUTNAM, A. (2014)
- MATSCHEI, C. (2012)
- PUSCHMANN, W., ZSCHEILE, D., & ZSCHEILE, K. (2009)
- SHACKLETON, D.M. (1997)
- TOKIDA, K. (2020). Capricornis crispus. The IUCN Red List of Threatened Species 2020: e.T3811A22151909. https://dx.doi.org/10.2305/IUCN.UK.2020-2.RLTS.T3811A22151909.en. Accessed on 23 January 2023.
- WEIGL, R. (2005)
- WILSON, D. E. et al. eds. (2009-2019)
- WILSON, D. E. & REEDER, D. M. (2005)
- YAMAMOTO, S. (1967)
- DAMOIS, P., ROBOVSKÝ, J., MUELLER, D, PENELLO, M.,ZIMMERMANN,M., VAN DER MEER, R.AND VOORHAM, M. (eds., 2020).
Zurück zu Übersicht Paarzeher
Weiter zu Indochina-Serau (Capricornis maritimus)