NICOLAÏ, M.P.J, PORCHETTA, S., BALAKRISHNA, S., BOTHA, D.P. & KOK, P.J.R. (2017)
Preliminary observations on the circadian variation in site fidelity in Atelopus hoogmoedi (Lescure, 1974) (Anura, Bufonidae).
Amphibian & Reptile Conservation 11(1) [General Section]: 45–50 (e136).
Inhalt:
Anhand von 14 markierten Männchen wurde die Ortstreue von Atelopus hoogmoedi überprüft.
"In conclusion our observations, although sparse, seem to confirm that Atelopus hoogmoedi does indeed show strong diurnal and nocturnal site fidelity, during breeding and non-breeding seasons. Although several hypotheses may explain this, the fact that perch site return rate is the highest after dark supports the predation evasion hypothesis."
nicolai-biblio
SCHMIDT, A. A. (1976)
Zur Nachzucht von Bufo blombergi (Salientia, Bufonidae).
Salamandra 12(1): 37-46.
Zusammenfassung:
Es wird von einer Laichabgabe von drei Paaren Bufo blombergi mit einer Gesamtzahl von ca. 50 000 Eiern am 25. und 26. XI. 1975 berichtet. Die Befruchtungsquote ist trotz dieses bisher in Gefangenschaft besten Ergebnisses mit 2 074 Quappen gering. Am achten Tag der Entwicklung schwammen die Quappen frei im Behälter. Die Hinterbeinansätze waren am 16. Tage erkennbar. Ab dem 36. Tag begann der Durchbruch der Vorderbeine. Vom 43. bis zum 47. 'Tag erfolgte die Metamorphose. Die umgewandelten Tiere verließen als kleine Kröten von 1 cm Länge das Wasser.
Die Wassertemperatur betrug 24°C, und die Quappen wurden mit Zierfischfutter der Marken Tetra Min, Tetra Ovin, Tetra Phyll , sowie mit Tabi Min Tabletten im Wechsel gefüttert. Die jungen Kröten, die am 13. II. 1976 bereits 2 cm Kopf-Steißlänge messen, sind leicht mit kleinen Grillen (Gryllus bimaculatus), Essigfliegen (Drosophila melanogaster), roten Mückenlarven (Chironomus sp .) und Larven der Wachsmotte (Galleria mellonella) zu ernähren. Die Aufzucht der Quappen einschließlich der Metamorphose verlief ohne nennenswerte Verluste. Auf starke Durchlüftung des Wassers während der Entwicklung der Quappen wurde besonderer Wert gelegt.
schmidt-biblio
VOGT, P . (1974)
Breeding and rearing the Colombian giant toad Bufo blombergi.
Internat. Zoo Yearb., 14: 87-90. London.
Inhalt:
Es wird über die erfolgreiche Zucht der Kolumbianischen Riesenkröte (heute = Rhaebo blombergi) im Jahr 1972 und die Auzucht der Jungtiere berichtet.
vogt-biblio
Kolumbianische Riesenkröte
Ordnung: Froschlurche (Anura)
Unterordnung: Moderne Froschlurche (Neobatrachia)
Familie: Kröten und Stummelfüße (Bufonidae)

Kolumbianische Riesenkröte
(Bufo =) Rhaebo blombergi • The Blomberg's Toad • Le craupaud de Blomberg
- Körperbau und Körperfunktionen
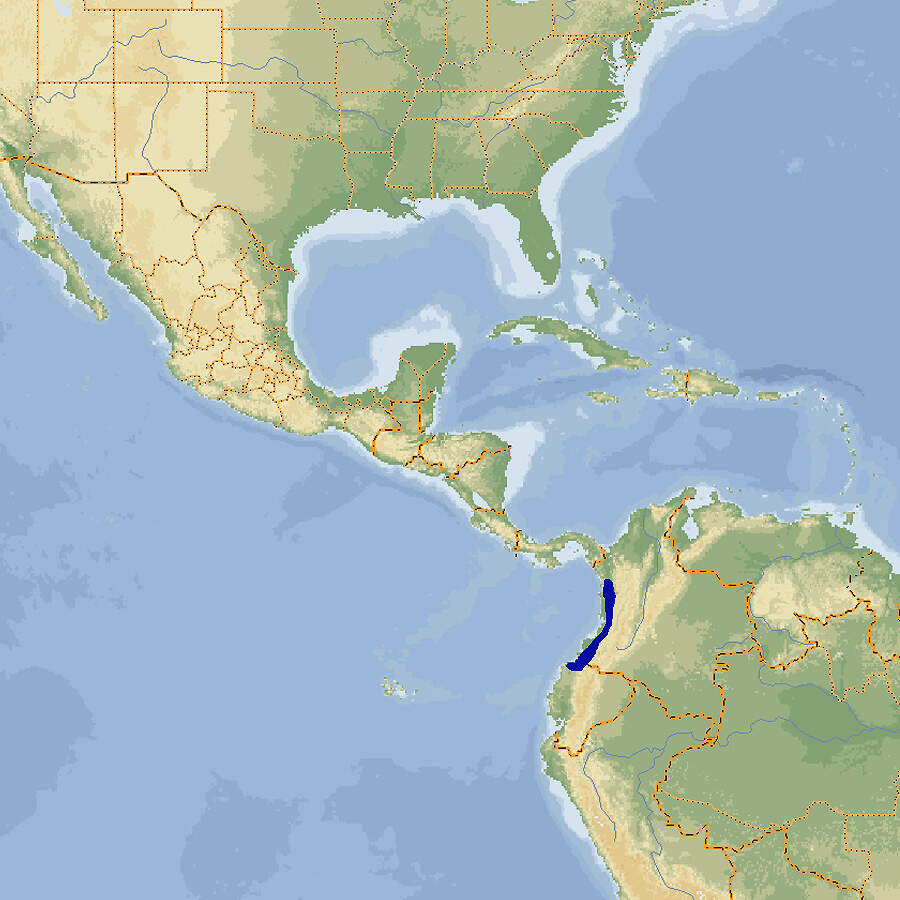
- Verbreitung
- Lebensraum und Lebensweise
- Gefährdung und Schutz
- Bedeutung für den Menschen
- Haltung
- Taxonomie und Nomenklatur
- Literatur und Internetquellen
|
Weitere Bilder auf BioLib |
Die erst 1950 entdeckte Kolumbianische Riesenkröte ist die größte Kröte überhaupt. Sie war deshalb bei Terrarianern sehr begehrt, entsprechend häufig im Handel und auch in Zoos anzutreffen. Mittlerweile ist die als potenziell gefährdet geltende Art aus europäischen Zoos vollständig verschwunden. Körperbau und KörperfunktionenDie Kolumbianische Riesenkröte ist mit einer Länge von 15-17 cm bei den Männchen und 20-25 cm bei den Weibchen der größte Vertreter der Bufoniden. Sie hat kurze Beine, Zehen ohne erweiterte Scheiben, einen dunkelbraune Iris und große, ovale Ohrspeicheldrüsen. Es fehlen entwickelte Schädelkämme. Die Haut an Rücken und Bauch ist größtenteils glatt. Rücken und Oberkopf sind hellbraun gefärbt, Kopf- und Körperseiten sowie die Beine dunkelbraun, der Bauch wiederum heller [2; 5]. VerbreitungSüdamerika: Von Nord-Ekuador bis West-Kolumbien auf der Pazifikseite der Cordillera Occidental [3; 5]. Lebensraum und LebensweiseDie Kolumbianische Riesenkröte bewohnt primäre Tropenwälder oder Sekundärwälder mit gutem Unterwuchs und wenig menschlichem Eingriff. Sie ist tag- und nachtaktiv. Jungtiere halten sich an den Ufern von Fließgewässern auf. Adulte kommen zur Fortpflanzung zu temporären oder permanenten Tümpeln oder Weihern in Flussnähe, ansonsten leben sie auch tief im Inneren der Wälder. Ein Weibchen produziert pro Fortpflanzungsperiode bis 80'000 (durchschnittlich 34'500) 1-2 mm große Eier, die in langen Laichschnüren abgelegt werden [2; 3; 5; 6; 7; 8]. Gefährdung und SchutzDie Kolumbianische Riesenkröte hat eine recht kleine Verbreitung, die etwa der Fläche Hessens oder Medcklenburg-Vorpommerns entspricht, und die Qualität ihres Lebensraums nimmt ab. Sie ist gilt daher nach einer revisionsbedürftigen Beurteilung aus dem Jahr 2004 als potenziell gefährdet (Rote Liste: NEAR THREATENED) [3]. Der internationale Handel ist durch CITES nicht geregelt. Bedeutung für den MenschenDie Art befindet sich für die Zwecke der Liebhaberei und der pharmazeutischen Forschung im internationalen Tierhandel [3; 4]. HaltungHaltung in europäischen Zoos: Die Art war in den 1960/70er Jahren relativ häufig in Zoos anzutreffen. 1972 gelang in Krefeld die vermutliche Welterstzucht in einem Zoo [7; 8]. Nach dem Jahr 2000 gab es nur noch vereinzelte Haltungen, und mittlerweile gibt es in europäischen Zoos wahrscheinlich keine mehr. Für Details siehe Zootierliste. Mindestanforderungen an Gehege: In Deutschland gibt es keine konkreten Mindestanforderungen. In Österreich sind diese in Anlage 4 der 2. Tierhaltungsverordnung, in der Schweiz in Anhang 2, Tabelle 6 der Tierschutzverordnung festgelegt. Taxonomie und NomenklaturDie Kolumbianische Riesenkröte wurde erst 1950 von dem schwedischen Forschungsreisenden Rolf BLOMBERG entdeckt und 1951 von den amerikanischen Zoologen George Sprague MYERS und John William FUNKHOUSER wissenschaftlich beschrieben und zu Ehren ihres Entdecker Bufo blombergi benannt. Im Zuge der Aufspaltung der Gattung Bufo kam sie 2006 in die von Edward Drinker COPE 1862 aufgestellte Gattung Rhaebo, die in der Folge zeitweilig als Untergattung aufgefasst wurde [1; 2; 5]. |
Literatur und Internetquellen
- AMPHIBIAN SPECIES OF THE WORLD
- AMPHIBIAWEB
- BOLÍVAR, W., COLOMA, L. A., RON, S. & CISNEROS-HEREDIA, D. (2004). Rhaebo blombergi. The IUCN Red List of Threatened Species 2004: e.T54590A11157227. https://dx.doi.org/10.2305/IUCN.UK.2004.RLTS.T54590A11157227.en. Accessed on 21 November 2022.
- GRZIMEK, B. (Hrsg. 1970)
- JAMBATU
- HERRMANN, H. J. (2005)
- SCHMIDT, A. A. (1976)
- VOGT, P . (1974)
Zurück zu Übersicht Stummelfüße und Kröten
Weiter zu Erdkröte (Bufo bufo)
Zipfelkrötenfrosch
 |
Neue Tierart
|
Ordnung: Froschlurche (Anura)
Unterordnung: Mittelalte Froschlurche (Mesobatrachia)
Überfamilie: Krötenfrösche (Pelobatoidea)
Familie: Asiatische Krötenfrösche (Megophryidae)
Unterfamilie: Megophryinae
Zipfelkrötenfrosch
Megophrys nasuta = Pelobatrachus nasutus • The Long-nosed horned frog •
La grenouille cornue asiatique
- Körperbau und Körperfunktionen
- Verbreitung
- Lebensraum und Lebensweise
- Gefährdung und Schutz
- Bedeutung für den Menschen
- Haltung
- Taxonomie und Nomenklatur
- Literatur und Internetquellen
|
Weitere Bilder auf BioLib
|
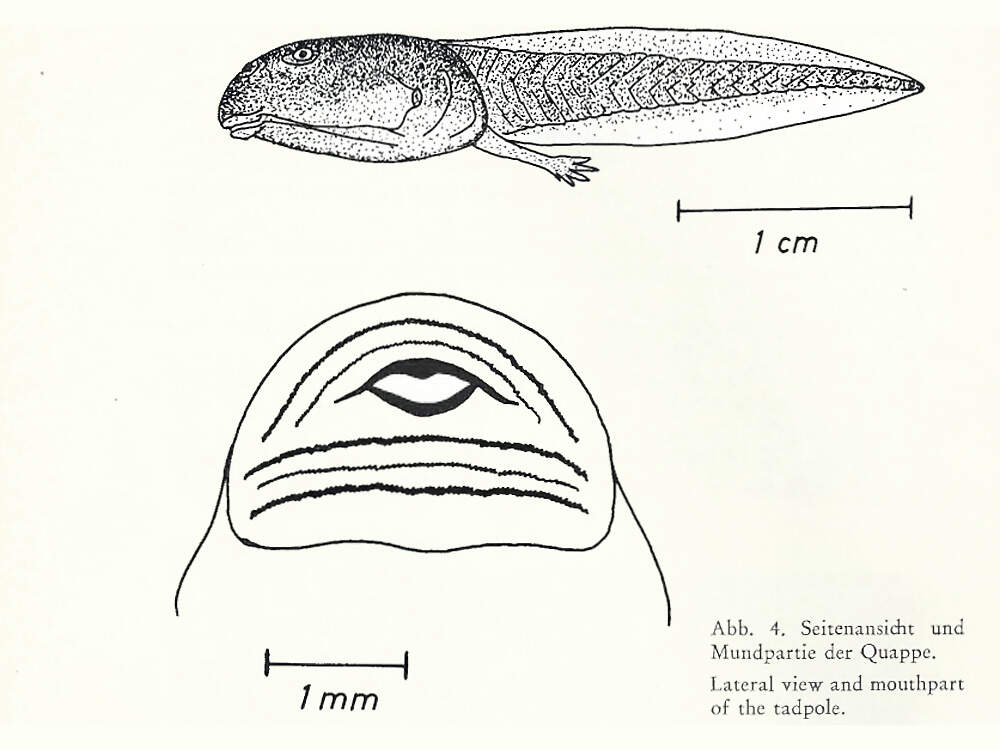
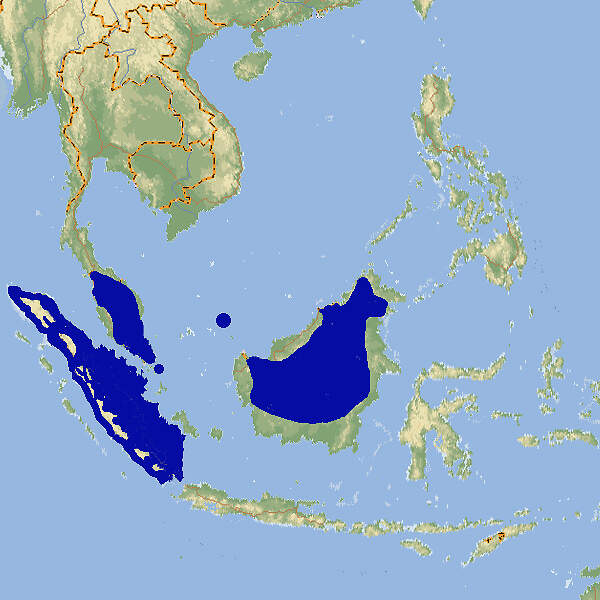
Der Zipfelkrötenfrosch ist eine nicht als gefährdet angesehene Art aus Südostasien. Wegen seines spektakulären Aussehens eignet er sich im Prinzip gut als Botschafter für seinen gefährdeten Lebensraum, die Regenwälder des malaiisch-indonesischen Tieflands. Allerdings ist sind die Tiere nachtaktiv und verstecken sich tagsüber häufig. Due Art wird deshalb regelmäßig in europäischen Zoos gezeigt, abr nicht in sehr vielen Haltungen. Körperbau und KörperfunktionenDer Zipfelkrötenfrosch, nicht zu verwechseln mit der Zipfelkröte (Sclerophrys superciliaris), verdankt seinen Namen den auffälligen, zipfelförmigen Auswüchsen über den Augen. Auch die Nase trägt einen spitzen Fortsatz. Weibchen werden bis ca. 12.5-16 cm lang. Männchen bleiben deutlich kleiner, selten sind sie mehr als halb so groß wie die Weibchen, maximal erreichen sie 10.5 cm. Von oben betrachtet ähnelt der Zipfelkrötenfrosch mit seiner Färbung, Gesamtform und sogar wie Blattadern aussehenden epidermalen Wucherungen einem Blatt. Dadurch wird er auf dem Waldboden nahezu unsichtbar. Er hat eine stark drüsige Haut, hauptsächlich in den Bereichen von Achseln, Brust- und Oberschenkeln [3; 7]. VerbreitungSüdostasien: Brunei, Indonesien (Sumatra, Kalimantan), Malaysia (Halbinsel, Sabah, Sarawak), Singapur, Thailand (marginal) [4]. Lebensraum und LebensweiseDer Zipfelkrötenfrosch besiedelt intakte Tiefland- und submontane Regenwälder bis in Höhenlagen von 1'300 m, meist in der Nähe von Waldbächen. Mit Störungen seines Lebensraums kommt er nur schlecht zurecht. Ausgewachsene Tiere leben an Land, die Kaulquappen in klaren Waldbächen. Die Tiere sind nachtaktiv und schlechte Springer, sondern ziehen es vor, zu gehen. Das Beutespektrum besteht hauptsächlich aus nestjungen Nagetieren, Echsen, Fröschen, Krabben, Skorpionen und Spinnen [3; 4; 7]. Die Eiablage erfolgt nach Einsetzen der Regenzeit im Wasser. Die Gelege umfassen rund 50-300 Eier. Die Kaulquappen schlüpfen etwa eine Woche nach Eiablage. Die Dauer bis zum Abschluss der Metamorphose ist temperaturabhängig und beträgt 2.5-3.5 Monate. Die Zipfel über den Augen beginnen sich etwa 2-3 Wochen später zu entwickeln [6; 7]. Gefährdung und SchutzDie Art ist weit verbreitet und offenbar häufig. Sie wurde daher aufgrund einer Beurteilung aus dem Jahr 2014, überprüft 2020, als global nicht-gefährdet taxiert. In der Roten Liste Singapurs aus dem Jahr 2011 wird sie jedoch als stark gefährdet eingestuft [2; 4]. Der internationale Handel wird durch CITESnicht geregelt. Bedeutung für den MenschenDer Zipfelkrötenfrosch wird in mäßigem Umfang für den Heimtierhandel gesammelt und exportiert. Abgesehen davon wird er lokal in Schmetterlingsfarmen ausgestellt [4]. HaltungWegen Kannibalismusgefahr wird empfohlen, unterschiedlich große Tiere einzeln zu halten oder sie nur zur Paarung zu vergesellschaften. Der Behälter sollte mindestens 80 cm lang sein und 15 cm tiefes Bodensubstrat aufweisen, damit sich die Tiere eingraben können [5]. Haltung in europäischen Zoos: Die Art wird regelmäßig, aber nicht sehr häufig in europäischen Zoos gezeigt. Nach Zootierliste liegt die Zahl der Haltungen gegenwärtig (2022) bei 16, davon 7 im deutschsprachigen Raum. Zoogestützte Forschung: Die Larvenentwicklung des Krötenzipfelfroschs wurde am Kölner Zoo erforscht [6; 7]. Mindestanforderungen an Gehege: In Deutschland gibt es keine konkreten Mindestanforderungen. In Österreich sind diese in Anlage 4 der 2. Tierhaltungsverordnung, in der Schweiz in Anhang 2, Tabelle 6 der Tierschutzverordnung festgelegt. Taxonomie und NomenklaturDer Zipfelkrötenfrosch wurde 1885 von dem aus Thüringen stammenden, am Naturhistorischen Museum Leiden tätigen Zoologen Hermann SCHLEGEL unter der Bezeichnung "Ceratophyne nasuta" erstmals wissenschaftlich beschrieben. 1873 stellte ihn der aus Esslingen stammende und am Natural History Museum in London tätige Zoologe Albert Carl Ludwig Gotthilf GÜNTHER in die Gattung Megophrys, die bis 2021 allgemein verwendet wurde. 2021 stellte ihn ein chinesisches Autorenteam, wie 1908 schon der englische Zoologe Frank Evers BEDDARD, in die Gattung Pelobatrachus, was aber von der IUCN nicht anerkannt wird [1; 2; 4]. |
Literatur und Internetquellen
- AMPHIBIAN SPECIES OF THE WORLD
- AMPHIBIAWEB
- ANIMAL DIVERSITY WEB
- IUCN SSC AMPHIBIAN SPECIALIST GROUP (2021). Megophrys nasuta. The IUCN Red List of Threatened Species 2021: e.T57582A114918773. https://dx.doi.org/10.2305/IUCN.UK.2021-3.RLTS.T57582A114918773.en . Accessed on 12 October 2022.
- TERRARISTIK FORUM
- VAN DER STRAETEN, K., KARBE, D., OLBORT, S. & T. ZIEGLER (2007): Erste Nachzucht des Zipfelkrötenfrosches, Megophrys nasuta, im Aquarium des Kölner Zoos. Terraria Nr. 6 2(4): 45-51.
- WILDENHUES, M., RAUHAUS, A., BACH, R., KARBE, D., VAN DER STRAETEN, K., HERTWIG, S. T. & T. ZIEGLER (2012). Husbandry, captive breeding, larval development and stages of the Malayan horned frog Megophrys nasuta (Schlegel, 1858) (Amphibia: Anura: Megophryidae). Amphibian and Reptile Conservation 6(1): 15-28.
Zurück zu Übersicht Stummelfüße und Kröten
Weiter zu Wechselkröte (Bufo = Bufotes viridis)
LAVILLA, E. O. & BRUSQUETTI, F. (2018)
On the identity of Bufo diptychus Cope, 1862 (Anura: Bufonidae).
Zootaxa 4442 (1): 161
ISSN 1175-5326 (Print Edition) & ISSN 1175-5334 (Online Edition)
Abstract:
The enigmatic toad Bufo diptychus was described by Cope (1862) based on a single individual (USNM 5841, now lost) of about 25 mm of SVL, collected during the expedition to La Plata River and tributaries, conducted by Captain Page between 1853 and 1856. As no dwarf species of toad was ever recorded in the surveyed area, and based on some tips that arise from Page’s narrative, we postulate that the description was based on a toadlet. With this hypothesis in mind, we compared Cope’s characterization of B. diptychus with juveniles of all species of Rhinella present in the region, finding an exact match in almost all characters shown by the juveniles of the common “cururú” or “rococo” toad, Rhinella schneideri (Werner 1894). Henceforth, we postulate that R. schneideri is a junior synonym of B. diptychus, under the combination Rhinella diptycha (Cope 1862).
lavilla-biblio
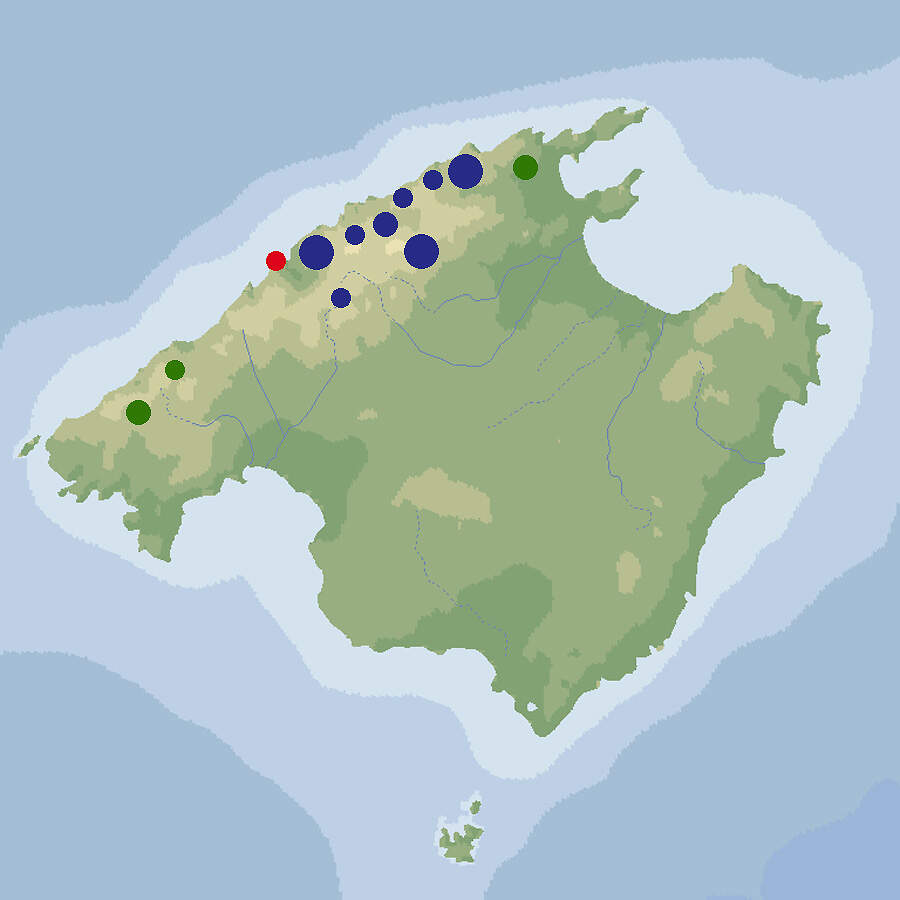
Mallorca-Geburtshelferkröte
Ordnung: Froschlurche (Anura)
Unterordnung: Urfrösche (Archaeobatrachia)
Familie: Scheibenzüngler (Alytidae / Discoglossidae)
Mallorca-Geburtshelferkröte
Alytes muletensis • The Majorcan Midwife Toad • L'alyte de Majorque
- Körperbau und Körperfunktionen
- Verbreitung
- Lebensraum und Lebensweise
- Gefährdung und Schutz
- Bedeutung für den Menschen
- Haltung
- Taxonomie und Nomenklatur
- Literatur und Internetquellen
|
Weitere Bilder auf BioLib
|
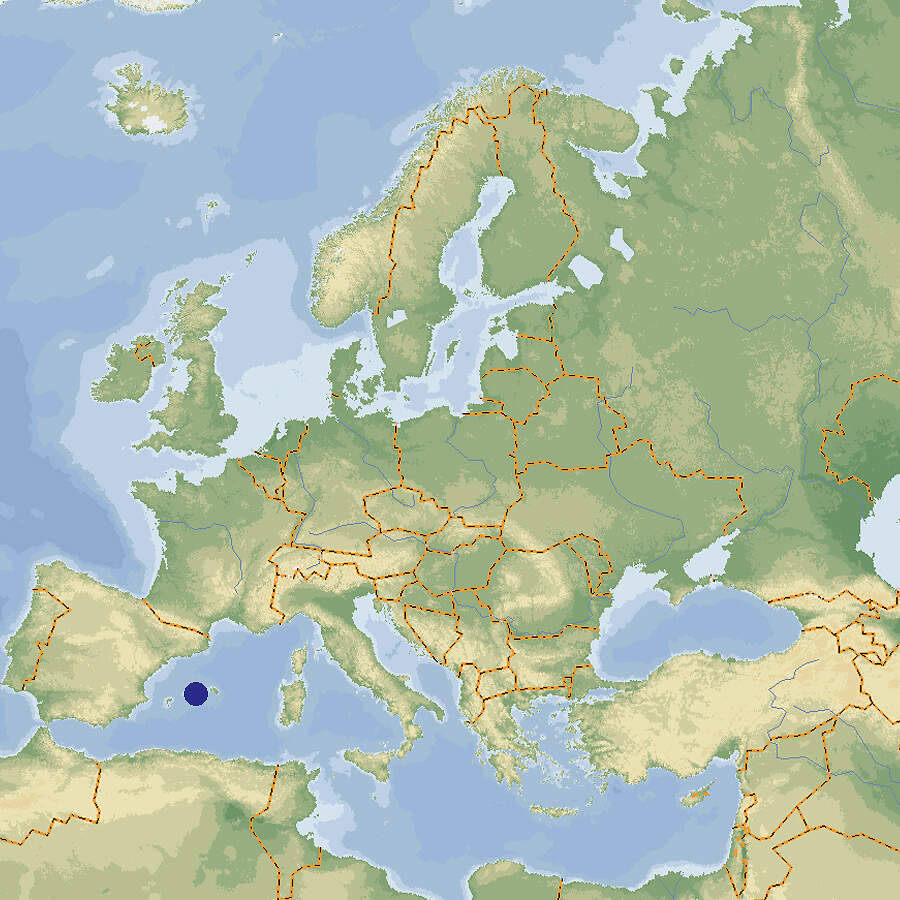
Die Mallorca-Geburtshelferkröte ist eine gefährdete Amphibienart, die auf aktiven Schutz in situ und ex situ angewiesen ist. Die Zahl der Zoos, welche die Art halten, ist zwar klein, aber diese sind engagiert und halten zum Teil recht große Bestände. Körperbau und KörperfunktionenDie Mallorca-Geburtshelferkröte ist eine kleine, gedrungene Kröte mit relativ großem Kopf und großen Augen mit vertikaler Schlitzpupille. Männchen werden ca. 35 mm, Weibchen ca. 38 mm lang. Damit sind sie kleiner als unsere einheimische Geburtshelferkröte. Das Gewicht erwachsener Tiere beträgt etwa 10-11 g. Im Vergleich zu anderen Alytes-Arten ist ihre Haut glatt und ist die Ohrdrüse schwach ausgebildet. Die Grundfarbe ist oberseits gelb oder cremefarben mit dunkelgrünen oder braunen Flecken und bisweilen einem schwarzen Dreieck auf dem Kopf. Der Bauch ist weiß [2; 3]. VerbreitungMallorca: Heute beschränkt auf ein kleines Areal in der Serra de Tramuntana im Norden der Insel [6]. Lebensraum und LebensweiseDie Mallorca-Geburtshelferkröte lebt in Höhenlagen von 10-850 m in Bächen, die in steilen Schluchten verlaufen, einige Bestände auch in vom Menschen gemachten Strukturen wie Wassertrögen auf Viehweiden oder Regenwassertanks. In ihrem natürlichen Lebensraum macht sie keine Winterruhe. Die Nahrung besteht aus Arthropoden aller Art, die sie hauptsächlich nachts fängt. Paarungen fnden im Sommer zwischen Juli und Ende August statt. Gelaicht wird in von den austrocknenden Bächen gebildeten Tümpeln oder anderen stehenden Kleingewässern. Die Gelege umfassen meist 8-12 bis zu 7 mm große Eier. Die Männchen tragen die Gelege, oft von mehr als einem Weibchen, während 3-4 Wochen. Danach kommt es erneut zu Paarung und Eiablage. Die Kaulquappen sind beim Schlupf etwa 18 mm lang und wachsen bis auf eine Länge von 77-88 mm. Die frisch metamophosierten Krötchen habe eine Länge von ca. 20.5 mm. Die Tiere könen ein Alter bis zu 18 Jahre erreichen [2; 3; 4; 7]. Gefährdung und SchutzDie Art wurde 2009 als gefährdet eingestuft (Rote Liste: VULNERABLE), weil sie ein kleines Areal von weniger als 20 km² hatte und ohne permanente Schutzanstrengungen in ihrem Bestand weiter abnehmen würde. Im Rahmen einer Neubeurteilung wurde sie 2020 in die Kategorie "stark gefährdet" (ENDANGERED) aufgenommen, weil die Lebensraumqualität und die Bestände weiterhin abnehmen. Zu den Gefährdungsursachen gehören die eingeführte Vipernatter (Natrix maura) als Fressfeind und der ebenfalls eingeführte Iberische Wasserfrosch (Pelophylax perezi) als Konkurrent und Fressfeind sowie wasserbauliche Maßnahmen [7]. Der internationale Handel ist durch CITES nicht geregelt. Die Geburtshelferkröte fällt unter Anhang II der Berner Konvention über die Erhaltung der europäischen wildlebenden Pflanzen und Tiere und ihrer natürlichen Lebensräume und ist in den Anhängen II und IV der FFH-Richtlinie (92/43/EWG) aufgeführt. Zoogestützte Schutzprojekte (Beispiele):
Bedeutung für den MenschenZur Erhaltung der Art werden in situ- und ex situ-Massnahmen getroffen. Eine Nutzung findet nicht statt. HaltungDie EAZA Amphibian TAG hat 2015 detaillierte Haltungsempfehlungen mit Angaben zu klimatischen Bedingungen und Fütterung herausgegeben. Für die Aufzucht der Kaulquappen ist mit etwa 1 l Wasser pro Individuum zu rechnen. Entsprechende Infrastruktur voausgesetzt, können bis zu 15 metamorphosierte Individuen auf 0.25 m² Fläche gehalten werden, wovon etwa ein Viertel Wasser sein soll. Im Fall einer Winterruhe werden Temperaturen von 8-14ºC angegeben [3; 4]. Haltung in europäischen Zoos: Die Art wird in weniger als 10 europäischen Einrichtungen gepflegt, auch im Tiergarten Schönbrunn, wo die Nachzucht regelmäßig gelingt. Für Details siehe Zootierliste. Mindestanforderungen an Gehege: In Deutschland gibt es keine konkreten Mindestanforderungen. In Österreich sind diese in Anlage 4 der 2. Tierhaltungsverordnung, in der Schweiz in Anhang 2, Tabelle 6 der Tierschutzverordnung festgelegt. Taxonomie und NomenklaturDie Mallorca-Geburtshelferkröte wurde erst 1979 von den Paläontologen Borja SANCHIZ und Rafel ANDROVER unter dem Namen "Baleaphryne muletensis" als ausgestorbene, subfossile Art erstmals wissenschaftlich beschrieben. Das Artepitheton "muletensis" bezieht sich auf den Fundort des Typus-Exemplars, die Cova de Muleta, eine Höhle in der Nähe von Port de Sóller im Nordwesten Mallorcas. Erst zwei Jahre später wurde festgestellt, dass die Art überlebt hatte, und 1984 wurde sie in die Gattung Alytes gestellt [1]. |
Literatur und Internetquellen
- AMPHIBIAN SPECIES OF THE WORLD
- AMPHIBIA WEB
- EAZA AMPHIBIAN TAG
- EUROPÄISCHE REPTILIEN UND AMPHIBIEN
- MAJORCA DAILY BULLETIN
- MARINELAND MALLORCA
- IUCN SSC AMPHIBIAN SPECIALIST GROUP (2020). Alytes muletensis. The IUCN Red List of Threatened Species 2020: e.T977A89697685. https://dx.doi.org/10.2305/IUCN.UK.2020-3.RLTS.T977A89697685.en. Downloaded on 19 December 2020.
Zurück zu Übersicht Zungenlose, Scheibenzüngler, Krötenfrösche
Weiter zu Geburtshelferkröte (Alytes obstetricans)
BAREJ, M. F., SCHMITZ, A., MENEGON, M., HILLERS, A., HINKEL, H., BÖHME, W. & RÖDEL, M. (2011)
Dusted off - The African Amietophrynus superciliaris-species complex of giant toads.
Zootaxa 2772: 1–32 (2011). www.mapress.com/zootaxa
Abstract:
Amietophrynus superciliaris is known to occur in rain forests from West Africa to eastern Democratic Republic of Congo and Gabon. We herein present morphological and molecular data indicating the existence of three distinct taxa. The name A. superciliaris superciliaris is restricted to toads from the western Lower Guinean Forest (eastern Nigeria, Cameroon, Equatorial Guinea, Gabon). We resurrect A. s. chevalieri for the Upper Guinean forest (Sierra Leone, Guinea, Liberia, Ivo-ry Coast, Ghana) and describe a new species occurring in the eastern part of the Lower Guinean Forest (eastern Demo-cratic Republic of Congo). Amietophrynus channingi sp. nov. from eastern Lower Guinean Forest differs from both other taxa by its brownish lateral coloration (reddish-purple in the other taxa). The new species differs morphologically from western Lower Guinean A. s. superciliaris by a less pointed eyelid process, a dark coloured posterior abdominal region and a dark coloured vertebral line (both absent in A. s. superciliaris), the shape of the parotid glands (bulged and rounded at the posterior tip in the new species, slender drop shaped and pointed at the posterior tip in A. s. superciliaris), and ju-venile interorbital markings (V-shaped in the new species, usually interrupted and broken in A. s. superciliaris). Amietophrynus channingi sp. nov. differs from the Upper Guinean A. s. chevalieri by the presence of an eyelid process (absent in A. s. chevalieri), presence of a dark vertebral line and a pair of dark spots on the posterior part of the back (both absent in A. s. chevalieri). The Upper Guinean A. s. chevalieri differs from western Lower Guinean A. s. superciliaris by the absence of an eyelid process, a dark coloured posterior abdominal region (absent in A. s. superciliaris) and lacking a pair of dark spots in the posterior part of the back (present in A. s. superciliaris). The new species differs from both other taxa by 2.2–2.8% in the investigated 16S rRNA gene. West African and western Central African populations differ by only 0.9–1.1% in 16S rRNA, lacking any intra-taxon variation within each clade, and are cautiously regarded as subspecies although the genetic distinction is mirrored by strong morphological differences and distinct geographic distribution which may support its elevation to species status once that more comprehensive data become available. A key to the taxa of the A. superciliaris-species complex is provided.
Dusted off - The African Amietophrynus superciliaris-species complex of giant toads (PDF Download Available). Available from: https://www.researchgate.net/publication/230555620_Dusted_off_-_The_African_Amietophrynus_superciliaris-species_complex_of_giant_toads [accessed Dec 06 2017].
BOULENGER, G. A. (1888)
List of the reptiles and batrachians collected by Mr. H. H. Johnston on the Rio del Rey, Cameroons District, W. Africa.
Proceedings of the Zoological Society of London 1887: 564–565.
Volltext
OHLER, A. & DUBOIS, A. (2016)
The identity of the South African toad Sclerophrys capensis Tschudi, 1838 (Amphibia, Anura).
PeerJ 4(e1553): 1–13.
Abstract:
The toad species Sclerophrys capensis Tschudi, 1838 was erected for a single specimen from South Africa which has never been properly studied and allocated to a known species. A morphometrical and morphological analysis of this specimen and its comparison with 75 toad specimens referred to five South African toad species allowed to allocate this specimen to the species currently known as Amietophrynus rangeri. In consequence, the nomen Sclerophrys must replace Amietophrynus as the valid nomen of the genus, and capensis as the valid nomen of the species. This work stresses the usefulness of natural history collections for solving taxonomic and nomenclatural problems.