Madagaskar
- Allgemeines, Vegetation, Tierwelt
- Typische Zootiere
- Nationalparks und andere Schutzgebiete
- Ankarafantsika-Nationalpark
- Mantadia-Andasibe-Nationalpark
- Marojejy-Nationalpark
- Masoala- und Nosy Mangabe-Nationalpark
- Integrales Naturschutzgebiet Betampona
- Weitere Schutzgebiete (Auswahl)
- Literatur und Internequellen
|
|
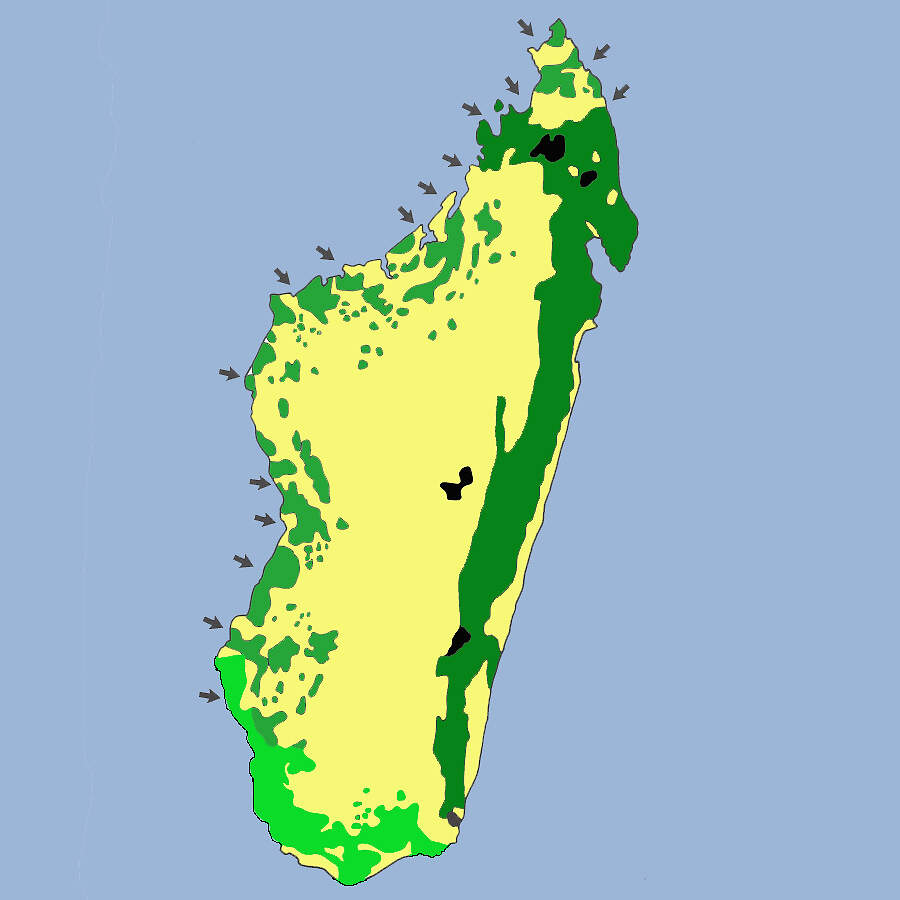
AllgemeinesMit einer Fläche von 587'000 km² (zum Vergleich: Deutschland 357'093 km²) ist Madagaskar nach Grönland, Neuguinea und Borneo die viertgrößte Insel der Erde, 1'600 km lang und bis 580 km breit. Im Zuge der Kontinentaldrift löste sich Madagaskar vor mehr als 65 Millionen Jahren vom afrikanischen Kontinent, was die Entwicklung einer eigenen Fauna und Flora mit einer Vielzahl endemischer Arten erlaubte. Die zentrale, im Mittel rund 1'100 m hohe Hochebene Madagaskars gewinnt von der Westküste her allmählich an Höhe und fällt dann nach Osten steil ab. Die von der Ostküste aufsteigenden Luftmassen kühlen sich daher ab und führen zu hohen Niederschlägen, sodass die Gegend ursprünglich von Regenwäldern bedeckt war. Im Westen herrscht dagegen ein arides Klima vor, in dem Sukkulenten gedeihen. Madagaskar kann grob in fünf bioklimatische Regionen unterteilt werden [9]:
Vegetation und CharakterpflanzenIn Madagaskar und den anderen Inseln des westlichen Indischen Ozeans kommen rund 12'000 Gefässpflanzen vor. Davon sind etwa 9'700 endemisch [7]. 4'735 madagasische Pflanzenarten sind in Rote Liste der IUCN erfasst. Davon gilt eine, Aloe silicola, als seit 1920 in der Natur ausgestorben, wird aber in Botanischen Gärten erhalten. 524 Arten sind unmittelbar vom Aussterben bedroht, 1'419 sind stark gefährdet, 898 gefährdet und 221 potenziell gefährdet [11]. Zur madagassichen Flora gehören der berühmte Baum der Reisenden, ein Strelitziengewächs, der Madagaskar-Schraubenbaum, die bei uns als Zimmerpflanze kultivierte Goldfruchtpalme (Dypsis lutescens) und zahlreiche weitere Palmenarten, z.B. etwa 20 endemische Arten der Gattung Ravenea, ferner Palm- und Baumfarne (Cycas, Alsophila), 8 verschiedenen Affenbrotbäume (Adansonia spp.), mehr als 1'000 Orchideenarten, darunter der Stern von Madagaskar (Angraecum sesquipedale). In den Trockengebieten des Westens und Südwestens wachsen zahlreiche Arten von Aloen, Euphorbien, einschließlich des Christusdorns, Pachypodien und Didieraceen (Alluaudia, Decarya, Didiera) [3; 6; 7; 9]. TierweltAnnähernd 5 % aller Tierarten weltweit, darunter fünf Familien von Primaten, sind hier endemisch. Die Lemuren leben ausschließlich auf Madagaskar und konnten sich hier ohne Konkurrenz zu anderen Primaten entwickeln. Seit der Ankunft des Menschen vor etwa 2'000 Jahren wurden 90 – 95 % des ursprünglichen Waldes auf Madagaskar zerstört, bei einer Abholzungsrate von ca. 100'000 ha pro Jahr. Von 107 bekannten, noch lebenden Lemurenarten sind 31 % vom Aussterben bedroht, 42% stark gefährdet und 23% gefährdet [10]. Aufgrund der vielen endemischen Arten und deren anhaltender Bedrohung durch massive Habitatzerstörung wurden die Primaten Madagaskars zu einer der höchsten globalen Naturschutzprioritäten erklärt (13, dort weiterführende Literatur). Nebst den Primaten leben auf Madagaskar und seinen Territorialgewässern 149 weitere Säugetierarten, davon sind 50 Flughunde und Fledermäuse. Nach Roter Liste der IUCN ausgestorben und nur von subfossilen Überresten bekannt sind ein oder zwei Riesen-Indri-Arten (Palaeopropithecus), die Riesenfossa (Cryptoprocta spelea) und zwei verzwergte Flusspferdformen (Hippopotamus guldbergi und Hippopotamus lemerlei) [7; 11]. Auf Madagaskar gibt es 248 Vogelarten, darunter 117 endemische. 2 Arten gelten als vom Aussterben bedroht, 17 als stark gefährdet, 19 als gefährdet und 13 als potenziell gefährdet. Im 19. Jahrhundert verschwand der Delalande-Seidenkuckuck (Coua delalandei) und in jüngster Zeit vermutlich ausgestorben ist der Alaotrataucher (Tachybaptus rufolavatus) [1; 11]. Die Herpetofauna ist durch 395 Reptilien- und 314 Amphibienarten vertreten. Bei den Reptilien handelt es sich um 381 Echsen und Schlangen, 13 Schildkröten, einschließlich Meeresschildkröten, sowie das Nilkrokodil. 24 Arten sind vom Aussterben bedroht, 54 sind stark gefährdet, 61 gefährdet und 46 potenziell gefährdet. Die Amphibien sind alles Froschlurche, bis auf 2 alles endemische, von denen 21 vom Aussterben bedroht, 80 stark gefährdet, 44 gefährdet und 18 potenziell gefährdet sind. Von den Fischarten der Binnen- und der marinen Territorialgewäßer werden 1'480 Knochen- und 91 Knorpelfische durch die Rote Liste erfasst. Bei den 52 stark gefährdeten, den 28 vom Aussterben bedrohten und den zwei bereits ausgestorbenen Arten handelt es sich mit wenigen Ausnahmen um Süßwasserfische, dabei stehen Buntbarsche (z.B. Paretroplus), Ährenfische (Bedotia) und Hechtlinge (Pachypanchax) im Vordergrund [2; 11]. |
Typische Zootiere
Nationalparks und andere Schutzgebiete
|
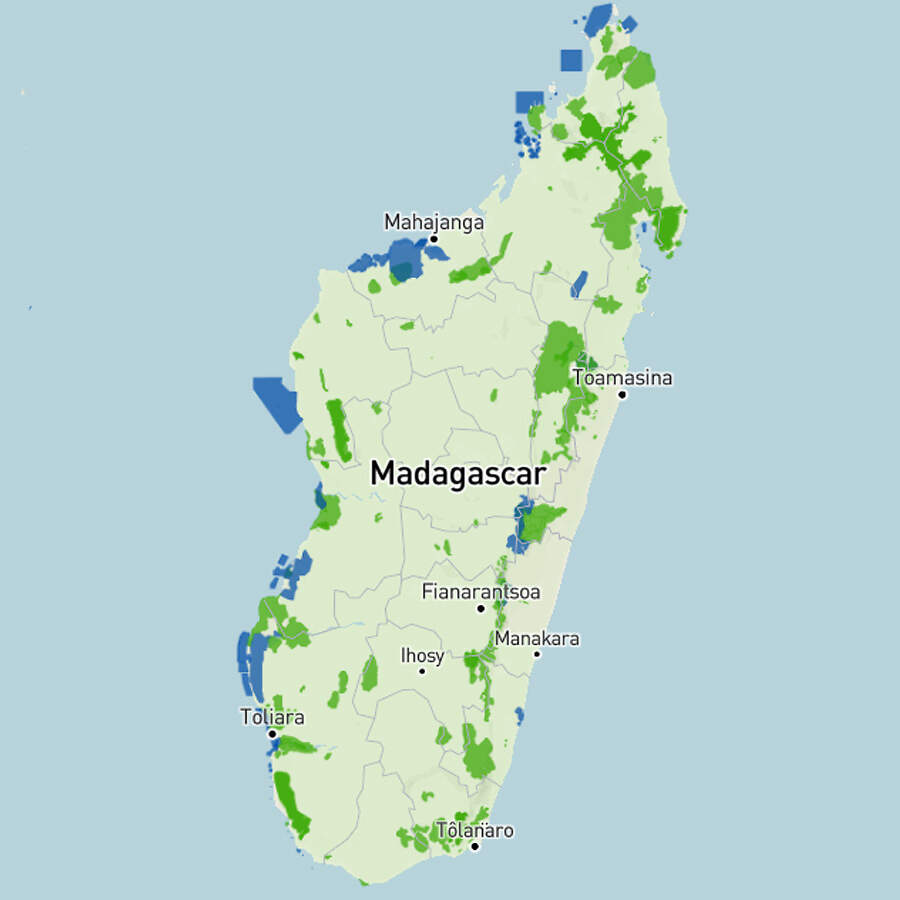
Madagaskar weist 171 Naturschutzgebiete auf, welche 44'521 km² (7.49%) der Landfläche und 11'018 km² (0.91% der Territorialgewässer) abdecken [10]. Davon werden 43 von der madagassischen Nationalparkverwaltung als Nationalparks, Meeres-Nationalparks, Sonderreservate ("Réserves spéciales") oder Integrale Naturschutzreservate ("Réserves naturelles intégrales") betrieben [8]. Sieben Parks gehören zum Weltnaturerbe, 2 Gebiete schützen nach Ramsar-Konvention Feuchtgebiete und Wasservögel und drei Parks sind Biosphärenreservate. BIRDLIFE INTERNATIONAL führt 84 ornithologisch bedeutsame Gebiete auf, von denen zahlreiche in Schutzgebieten liegen [1]. |
Ankarafantsika-Nationalpark, Nordwest-Madagaskar
|
|
Bestehend seit 2002. Das Gebiet besteht aus Trockenwäldern, Savannen, Kalksteinhügeln und Seen. Charakterpflanzen: Das Pflanzeninventar des Parks umfasst 823 Arten, von denen die allermeisten endemisch sind. Bei vielen Arten handelt es sich um Medizinalpflanzen. Besonders auffällige Gewächse sind: das bis 8 m hohe sukkulente Pachypodium rutembergianum, der Affenbrotbaum (Adansonia madagascariensis var. boinensis), verschiedene Palisanderhölzer (Dalbergia spp.), die als Medizinalpflanzen genutzten Bäume Baudouinia fluggeiformis, Cedrelopsis grevei und Strychnos myrtoïdes, sowie die Raffia-Palme (Raphia farinifera). Tierwelt: Im Park wurden 8 Lemurenarten beobachtet, darunter der nur hier vorkommende Goldbraune Mausmaki (Microcebus ravelobensis) sowie Schwarzkopfmaki, Mongozmaki und Coquerel-Sifaka (Propithecus coquereli). Die Raubtiere sind durch den Falanuk (Eupleres goudotii) und die Fossa vertreten, die Wälder des Parks sind das alleinige Areal der Ankarafantsika-Großfußmaus (Macrotarsomys ingens). Wegen seiner 129 Arten umfassenden Vogelwelt ist der Ankarafantsika-Nationalpark ein ornithologisch bedeutendes Gebiet (IBA MG027). Literatur und Internetquellen: [1; 8; 9] |
Mantadia-Andasibe-Nationalpark, Ost-Madagaskar
|
|
Bestehend seit 1989. Zum Park gehört auch das 810 ha große Analamazaotra-Sonderreservat. Die dichtbewaldete, hügelige Landschaft des Parks wird von zahlreichen kleinen Flussläufen durchbrochen, von denen einige aufgestaut wurden. Charakterpflanzen: Regenwald (größtenteils Sekundärwald) mit Palmen (Dypsis, Ravenea), Palisander- (Dalbergia), Ebenholz- (Diospyros), Lalona- (Weinmannia) und Schraubenbäumen. Es wurden über 1'200 Pflanzenarten nachgewiesen, von denen 77% endemisch sind, darunter befinden sich 120 endemische Orchideenarten. Tierwelt: Im Park leben 14 Lemurenarten, darunter Schwarzkopfmaki, Rotbauchmaki, Großer Bambuslemur, Östlicher Grauer Bambuslemur (Hapalemur griseus), Schwarzweißer Vari, Diademsifaka (Propithecus diadema), Indri (Indri indri), Wollmaki (Avahi laniger) und Fingertier, 58 andere Säugetiere, darunter Fossa, Fanaloka, Ringelschwanzmungo und Falanuk (Eupleres goudotii). Allein für das kleine Analamazaotra-Sonderreservat werden 11 Tanrek-Arten angegeben, darunter Kleiner Igeltanrek, Tiefland-Streifentanrek und Großer Tanrek, Wegen seiner artenreichen Vogelwelt ist das Reservat ein bedeutendes Vogelschutzgebiet, in dem über 117 Arten nachgewiesen wurden (IBA MG054). Darunter befinden sich Mähnenibis, Hovaralle (Sarothrura insularis), Madagaskar-Fruchttaube (Alectroenas madagascariensis), Madagaskar-Schleiereule (Tyto soumagnei), Blauer Seidenkuckuck, Rotstirn- (Coua reynaudii) und Rotbrust-Seidenkuckuck (C. serriana) sowie Blaukopf-Erdracke. 51, zu 95% endemische, Reptilien- und 84 Amphibienarten, von denen 98% endemisch sind, machen die Herpetofauna des Parks aus. Darunter befinden sich Parsons Chamäleon (Calumma parsonii), und die Frösche Aglyptodactylus madagascariensis, Boophis difficilis, Mantella pulchra, Mantidactylus grandidieri und Platypelis barbouri. Literatur und Internetquellen: [1; 4; 5; 8; 9, 10] |
Marojejy-Nationalpark, Nord-Madagaskar
|
|
Bestehend als Integrales Reservat seit 1952, als Nationalpark seit 1998 und als Weltnaturerbe seit 2007. Marojejy ist ein Gebirgsmassiv mit steilen Granitgipfeln, das zu 90% von Wald bedeckt ist. Dabei handelt es sich um Tiefland-Regenwald, feuchten immergrünen Wald der Hügelstufe und dichten Hartlaubwald der montanen Stufe. Darüber Buschland mit Baumheiden und alpine Rasen. Charakterpflanzen: Im Park kommen etwa 350 Farnarten vor, darunter Baumfarne (Alsophila alticola, A. boiviniiformis), 50 Palmenarten, einschließlich der vom Aussterben bedrohten Marojejya darainii, ferner u.a. Sternapfelbäume (Chrysophyllum sp.), Herzblättrige Feigen (Ficus polita) und Palisanderhölzer (Dalbergia baroni, D. louvelii). Tierwelt: Zu den im Park vorkommenden Säugetiere gehören 11 Lemurenarten, darunter Nördlicher Bambuslemur (Hapalemur occidentalis), Weißkopfmaki, Rotbauchmaki, Seidensifaka (Propithecus candidus), Indri (I. indri) und Fingertier, ferner Breitstreifenmungo (Galidictis fasciata), Fossa, Fanaloka und 25 verschiedene Kleinsäuger. Mit 96 Vogelarten, wovon 63 endemischen, gilt der Park als ornithologisch bedeutendes Gebiet (IBA MG016), und die Herpetofauna zählt 149 Arten. Literatur und Internetquellen: [1, 8, 9] |
Masoala- und Nosy Mangabe-Nationalpark, Nordost-Madagaskar
|
|
Bestehend als Nationalpark seit 1997 und als Weltnaturerbe seit 2007. Masoala schützt den größten zusammenhängenden Regenwald Madagaskars, bestehend aus Tiefland-, Hügel- und Bergregenwald, ferner Küstenwälder und Mangrovensümpfe. Zum Park gehören auch die 520 ha große, bis auf einen Campingplatz für Forscher und Touristen unbesiedelte Insel Nosy Mangabe in der Baie d’Antongil und die Meereschutzgebiete Tampolo, Ambodilaitry und Ifaho mit Sandstränden und Korallenriffen Charakterpflanzen: Im Park wurden ca. 1'100 Gefäßpflanzen nachgewiesen, in den Meeresschutzgebieten 99 Algenarten. Marojejya darainii, Dypsis pachyramea und Lemurophoenix halleuxi sind in Nordost-Madagaskar endemische Palmen. Nur auf der Halbinsel kommt die fleischfressende Kannenpflanze Nepenthes masoalensis vor. Auch Takhtajania perrieri, einen urtümlicher Strauch aus der Familie der Winteraceae gibt es hier. Auf der Masoala-Halbinsel gedeihen wertvolle Harthölzer, so über 25 Arten Ebenhölzer(Diospyros spp.) sowie Palisander-Arten (Dalbergia spp.) einschließlich Rosenholzbäume (Dalbergia latifolia, D. nigrescens und D. oliveri), die oft illegal geschlagen werden. Tierwelt: Im Masoala-Nationalpark sind 10-11 Arten von Halbaffen zuhause, darunter der Weißkopfmaki, der in den 1930er Jahren auf Nosy Mangabe angesiedelte Gürtelvari, Roter Vari, und Fingertier. Unter den 9 Raubtierarten befinden sich Fossa, Fanaloka, Ringelschwanzmungo , Schlichtmungo (Salanoia concolor) und Falanuk (Eupleres goudotii). Angesiedelt wurde das Afrikanische Buschschwein (Potamochoerus larvatus). In der Baie d'Antongil halten sich von Juli bis September Buckelwale (Megaptera novaeangliae) auf und gebären ihre Jungen. Verschiedene Delfinarten können während des ganzen Jahres beobachtet werden. Der Park ist ein bedeutendes Vogelschutzgebiet, in dem 111 Arten nachgewiesen wurden, davon 60 endemische (IBA MG017). Von besonderer Bedeutung ist er für den bedrohten Madagaskar-Schlangenhabicht (Eutriorchis astur). An Reptilien und Amphibien seien Pantherchamäleon und Großer Madagaskar-Taggecko sowie Tomatenfrosch und das Folohy-Buntfröschchen erwähnt. Literatur und Internetquellen: [1; 3; 8; 12] |
Integrales Naturschutzgebiet Betampona, Ost-Madagaskar
|
|
Bestehend seit 1927. Weltnaturerbe seit 2007. Das Gebiet liegt in hügeligem Gelände. Es wird von 12 Bächen durchflossen, die an mehreren Orten Wasserfälle aufweisen, und ist mit dichtem Regenwald besetzt. Vegetation und Charakterpflanzen: Es wurden 219 Gefäßpflanzen nachgewiesen (was wohl unvollständig ist), davon 141 Farn- und 25 Palmenarten, unter denen Dypsis tsaravotsira besondere Erwähnung findet. Tierwelt: Im Schutzgebiet leben 11 Lemuren, darunter Weißkopfmaki, Indri (Indri indri) und Diademsifaka (Propithecus diadema). Der Bestand an Schwarzweißen Varis wurde mit Tieren aus nordamerikanischen Haltungen aufgestockt. Ferner gibt es vier Raubtierarten: Fossa, Ringelschwanz-, Breitstreifen- (Galidictis fasciata) und Schlichtmungo (Salanoia concolor). Betampona ist ein ornithologisch bedeutendes Gebiet (IBA MG048), in dem 93 Vogelarten nachgewiesen wurden, davon 44 madagassische Endemiten. Anzutreffen sind u.a. Zwergtaucher, Glockenreiher (Egretta ardesiaca), Hammerkopf, Mähnenibis, Brauner Sichler, Perlwachtel, Madagaskartaube, Teichhuhn, Großer Vasapapagei, Grauköpfchen, Blauer und Spitzschopf-Seidenkuckuck, Schuppen-Erdracke (Brachypteracias squamigera), Helm- (Euryceros prevostii) und Schwarzvanga (Oriolia bernieri). Die Herpetofauna ist laut Nationalparkverwaltung mit 29 Reptilien- und 38 Amphibienarten vertreten. Literatur und Internetquellen: [1; 8; 9; 14] |
Weitere Schutzgebiete (Auswahl)
|
|
Nationalparks
Integrales Naturschutzgebiet
Sonder-Reservate
Andere
|
Literatur und Internetquellen
- BIRDLIFE DATA ZONE
- GLAW, F. & VENCES, M. (2007)
- GRAF, R. 2005
- LEMURS OF MADAGASCAR
- MADAGASKAR.DE
- MARRIED TO PLANTS
- MITTERMEIER, R.A., MYERS, N. & GOETTSCH-MITTERMEIER, C. (1999)
- PARCS MADAGASCAR
- PRESTON-MAFHAM, K. (1991)
- PROTECTED PLANET
- ROTE LISTE DER IUCN
- RÜBEL, A., HATCHWELL, M. & MACKINNON, J. (2003)
- SCHWITZER, C., SCHWITZER, N, RANDRIATHAHINA G. H. & KAUMANS, W. (2005)
- SEILER, M. & SCHWITZER, C. (2010)
- WWW.INATURALIST.ORG
Zurück zu Übersicht Meere, Inseln, Antarktis
Weiter zu Maskarenen
Inseln vor der Ostafrikanischen Küste
Unmittelbar vor der ostafrikanischen Küste liegen vier Inselgruppen: der Lamu-Archipel vor Kenia, der Sansibar-Archipel vor Tansania sowie der Quirimbas Archipel und der Basaruto-Archipel vor Mosambik.
Sansibar
|
|
AllgemeinesDer Sansibar-Archipel besteht aus der Hauptinsel Sansibar (Unguja), Pemba und Mafia mit ihren Nebeninseln, darunter das Atoll Mnemba, sowie die Koralleninsel Latham, die von einem Saumriff umgeben ist. Alle Inseln zusammen haben eine Fläche von etwa 3'200 km². Mit über 370 Einwohnern / km² ist der Archipel äußerst dicht besiedelt. Die Inseln sind ziemlich flach, die höchste Erhebung liegt 120 m.ü.M. Während der letzten Eiszeit waren sie mit dem Festland verbunden, was in der Säugetierfauna zum Ausdruck kommt. Sansibar ist Teil des Brennpunkts der Biodiversität "Ostafrikanische Gebirge und Küstenwälder". In den rund 1400 km² Küstenwald auf dem Festland und den Inseln kommen rund 600 endemische Pflanzen und 300 endemische Arten Land-Wirbeltiere vor, darunter Roter Sansibar-Stummelaffe (Procolobus kirkii), Sansibar-Galago (Galagoides), Sansibar-Ginsterkatze (Genetta servalina archeri), Aders-Ducker (Cephalophus adersi) und Pemba-Flughund (Pteropus voeltzkowi), ferner der Sansibar-Fiederbartwels (Synodontis zanzibaricus). Vegetation und CharakterpflanzenGroße Teile des Küstenwaldes Tansanias sind zwar nicht eigentliche Schutzgebiete, stehen aber unter dem Schutz der Forstgesetzgebung. Allerdings ist der Wald stark fragmentiert und besteht heute aus 165 einzelnen Wäldern, die im Mittel nur 850 ha umfassen. Charakteristische Baumarten sind Rosenholz (Calophyllum inophyllum), Schraubenbaum (Pandanus rabaiensis), Ölpalme (Elaeis guineensis). Den Mangrovenwald dominieren Rhizophora mucronata, Ceriops tagal und Avicennia marina. TierweltWegen der dichten Besiedlung und der starken Fragmentierung der Wälder können sich Populationen größerer Säugetiere kaum halten. So ist der Sansibar-Leopard vermutlich seit 1996 ausgestorben (Rote Liste der IUCN). Zwerggalago (Galago senegalensis zanzibaricus), Roter Sansibar-Stummelaffe, Sansibar-Diademmeerkatze (Cercopithecus mitis albogularis), Sansibar-Ginsterkatze, Sansibar-Ducker, sämtliche waldbewohnenden Vogelarten der Insel (IBA TZ057, 556 ha), wo insgesamt 217 Arten vorkommen, darunter Braunkopfpapagei (Poicephalus cryptoxanthus), Sansibarspecht (Mesopicos elliotii johnstoni), Sansibarwürger (Laniarius sublacteus), Blauflügelrötel (Sheppardia gunningi) und Brandweber (Euplectes nigroventris). Nationalparks und SchutzgebieteJozani Chwaka Bay National ParkAuf der Hauptinsel gibt es nur einen Nationalpark, in dem der Josaniwald liegt. Der Park mit einer Fläche von 50 km² liegt nur wenige Meter über Seehöhe. Es erhält ca. 850 mm Niederschlag / Jahr, die mittlere Monatstemperaturen beträgt tagsüber 28-32°C, nachts 18-23°C. Der Josani-Nationalpark umfasst einen noch recht ursprünglichen Grundwasserwald, Küstenwald, Mangroven, Buschland und Salzwiesen. Es sind so ziemlich die einzigen Überbleibsel dieser Pflanzengesellschaften, die einst ganz Sansibar bedeckten. Die Chwaka-Bucht ist ein Important Bird Area (TZ045), vor allem für Reiherläufer (Dromas ardeola), Wüstenregenpfeifer (Charadrius leschenaultii) und Orientseeschwalbe (Sterna saundersi). Mafia Island Marine Park1995 wurde der Mafia Island Marine Park ausgerufen, der mit einer Fläche von 821 km² hauptsächlich dem Schutz der Korallenriffe und mehr als 400 Fischarten dient. |
![]()
Literatur und Internetquellen
BIRDLIFE DATA ZONE
EICHLER, D. (1997)
KING, D. (1996)
MITTERMEIER, R.A., MYERS, N. & GOETTSCH-MITTERMEIER, C. (1999)
Zurück zu Übersicht Meere, Inseln, Antarktis
Weiter zu Madagaskar
Nationalparks in Malaysia
Nationalparks und andere Schutzgebiete
Tabin-Wildschutzgebiet
.jpg)
Selektiv eingeschlagener Tieflandregenwald im Tabin-Reservat, Sabah, Malaysia © Frank OberwemmerSabah, Malaysia
Errichtet 1983. 122'539 ha, 100 - 571 m.ü.M.
Jahresniederschlag 2'000-3'000 mm
Important Bird Area MY027
Vegetation: Relikte von primärem Tiefland-Regenwald, hauptsächlich Sekundärwälder, ferner etwa 100 ha .jpg)
Selektiv eingeschlagener Tieflandregenwald im Tabin-Reservat, Sabah, Malaysia © Frank OberwemmerSumpfwald und 200 ha Mangroven. Mindestens 1300 nachgewiesenen Arten.
Tierwelt: Javaner-, Schweins- und Nasenaffe, Hose-Langur (Presbytis hosei), Maronenlangur (Presbytis rubicunda), Borneo-Gibbon, Borneo-Orang, Malaienbär, Bengalkatze, Flachkopfkatze (Prionailurus planiceps), Borneo-Goldkatze (Pardofelis badia), Marmorkatze (Pardofelis marmorata), Nebelparder (Neofelis diardi), große Population des Asiatischen Elefanten, Sumatranashorn (†), Kantschil, Muntjak, Sambar, Banteng, ca. 260 Vogelarten, darunter Höckerstorch (Ciconia stormi), Zwerghaubenadler (Nisaetus nanus), Große Grüntaube (Treron capellei), Brustband-Eisvogel (Alcedo euryzona), Rotrückenpitta (Pitta baudii) und weitere gefährdete Arten.
Taman Negara-Nationalpark
.jpg)
Taman Negara-Nationalpark, Malaysia © Jonathan Kelly
Bundesstaaten Pahang, Kelantan und Terengganu, Malaysia
Gegründet 1938/39. 431'453 ha. Hügelig (75-300 m.ü.M.), im Zentrum gebirgig (bis 2187 m.ü.M.)
Vegetation: Tropischer Regen- und Höhenwald .
Tierwelt: 120 Säugetierarten, darunter Weißhandgibbon, Rothund, Buntmarder, Leopard, Malaiischer Tiger, Asiatischer .jpg)
Morgennebel im Taman Negara-Nationalpark, Malaysia © Jonathan KellyElefant, Schabrackentapir, Sumatranashorn (†), Kantschil, Muntjak, Sambar, Gaur. Über 300 Vogelarten, darunter Schwarzwachtel (Melanoperdix nigra), Gelbschwanzfasan (Lophura erythrophthalma), Rothschild-Pfaufasan (Polyplectron inopinatum), Malayischer Pfaufasan (Polyplectron malacense), Perlenpfau (Rheinardia ocellata), Argusfasan (Argusianus argus), Höckerstorch (Ciconia stormi), Zwerghaubenadler (Nisaetus nanus) und weitere gefährdete Arten. 67 Schlangen-, 55 Frosch- und 109 Süßwasserfischarten.
![]()
Literatur und Internetquellen:
BEHLER, N. (2012)
GARDNER; P. C., AMBU, K., BERNARD, H. & GOOSSENS, B. (1914)
MITTERMEIER, R.A., MYERS, N. & GOETTSCH-MITTERMEIER, C. (1999)
PFEFFER, P. (1969)
WWF Malaysia & Cubitt, G. (1998)
BirdLife International (2013) Important Bird Areas factsheet: Tabin Wildlife Reserve.
BirdLife International (2013) Important Bird Areas factsheet: Taman Negara National Park.
Zurück zu Lebensräume in Süd- und Südostasien
Weiter zu Wallacea
Nationalparks in Indonesien
Komodo-Nationalpark
Errichtet: 1980
Gesamtfläche: 2193.22 km², davon rund ein Drittel Land
Höhenlagen: 0-735 m auf Komodo, bis 667 m auf Rinca
Temperatur: Mittlere Temperaturen von 17 bis 34°C. Während der Trockenzeit liegen die Höchsttemperaturen bei ca. 40°C
Jahresniederschlag: ca. 800-1000 mm
Der Komodo-Nationalpark liegt westlich von Flores. Er besteht aus einem Stück der Westküste von Flores, den Inseln Komodo (339.37 km²), Rintja oder Rinca (196.25 km²) und Padar (20.17 km²), Gili Motang (ca 30 km²), Gili Dasami, zwei Dutzend kleineren Inselchen und dem umgebenden Meeresgebiet.
Die allgemeine Topografie ist hügelig, die Küste ist felsig mit Sandstränden in geschützten Buchten.
Vegetation: Etwa 70 % der Insel sind mit Savanne bedeckt mit der Palmyra- oder Lontarpalme (Borassus flabellifer) als wichtigster Baumart, ferner gibt es am Fuß der Hügel und in den Tälern Monsunwälder mit überwiegend laubabwerfenden Bäumen, darunter Stinkbaum (Sterculia foetida), Mandukbaum (Oroxylum indicum), Tamarindenbaum (Tamarindus indica), Jujube (Zizyphus horsfeldi), Schleichera oleosa, Cassia indica, Nebelwälder mit zahlreichen Endemiten in Höhenlagen über 500 m und Mangrovenwälder.
Tierwelt: Reichhaltige Meeresfauna mit Korallenriffen, Haien, fünf Arten Meeresschildkröten, Blau-, sei und Pottwalen, zehn Delfinarten und Dugongs (Dugong dugon). An Land nebst den unten genannten typischen Zootieren u.a. Timor-Ochsenfrosch (Kaloula baleata), Freycinet-Großfußhuhn (Megapodius freycinet), ein Flughund (Pteropus electa) und verschiedene andere Fledertiere, Reisratte (Rattus exulans), Rincaratte (Rattus rintijanus). Important Bird Area ID 124 mit u.a. Flores-Grüntaube (Treron floris), Floreskrähe (Corvus florensis).
Typische Zootiere:
- Komodowaran
- Weißlippen-Bambusotter
- Gelbwangenkakadu
- Javaneraffe
- Fleckenmusang
- Wildschwein
- Timorhirsch
- Wasserbüffel (verwildert)
![]()
Literatur und Internetquellen:
PETER, W. & HOHMANN, G. (1983)
BIRDLIFE DATA ZONE
Komodo Island is the NEW 7 Wonders of The World
WORLD HERITAGE NOMINATION - IUCN Summary
Zurück zu Indomalaiischer Archipel
Weiter zu Wallacea
DOLLINGER, P. (Hrsg., 2014)
Wie kommen Zoos zu guten Führungskräften?
Verhandlungsbericht des VI. Rigi-Symposiums, gemeinsam organisiert von ZOOSchweiz, OZO und Zoos in Bayern, Goldau-Rigi, 30. Januar - 2. Februar 2014. Zoo Office Bern. 89 Seiten.
Editorial:
"Es gibt keine schlechten Mannschaften, Marschall. Es gibt nur schlechte Offiziere."
Napoleon I. Bonaparte
Zoodirektor erscheint vielen als Traumberuf. Sich den ganzen Tag um Tiere zu kümmern und sich im Rampenlicht der Öffentlichkeit zu sonnen, was gibt es Schöneres?
Die Realität sieht allerdings anders aus – nicht so wie auf den Titelbildchen zu den einzelnen Artikeln dieses Bandes, wo wir die Damen und Herren Zoodirektoren zusammen mit Tieren abgebildet haben. Vielfach wird der Direktor durch administrative Belange so belastet, dass kaum noch Zeit für direkte Kontakte mit Tieren bleibt. Und die Zeiten, wo der Direktor jeden Morgen mit den leitenden Mitarbeitern „auf die Runde“ ging und alle Gehege inspizierte, sind in den meisten Zoos auch schon vorbei.
Dass der Zoodirektor – oder die Zoodirektorin, denn heute werden im Verband der Zoologischen Gärten (VdZ) bereits ein Viertel der Mitgliedzoos von Frauen geleitet – eine öffentliche Person ist, trifft dagegen zu. Allerdings ist das nicht immer positiv. Denn mittlerweile gibt es eine zwar kleine, aber umso lautstärkere Gruppe von Leuten, die die Haltung und Nutzung von Tieren - und damit auch Zoos - grundsätzlich ablehnen. Diese Leute fokussieren ihre Kritik lieber auf den stadtbekannten Zoodirektor, mit dem sie mehr Medieninteresse generieren können, als mit Landwirt Hinz oder Katzenhalterin Kunz. Nachdem heute viele Medienvertreter unter „kritischem Journalismus“ hauptsächlich verstehen, dass sie Kritikern von vornherein recht geben, ohne zu überprüfen, wie fundiert deren Kritik ist, wird aus dem Zoodirektor leicht einmal ein „umstrittener Zoodirektor“ und aus diesem ein „umstrittener ehemaliger Zoodirektor.
Zudem haben Zoodirektoren ein breites Spektrum an Aufgaben zu bewältigen für das sie Wissen und Kompetenzen benötigen. Sie sind nämlich nicht nur Vorgesetzte, Manager, Politiker, Mediatoren und Kommunikatoren sondern auch Masterplaner, Bauherren und Fundraiser, und müssen sich in Fragen der Zoologie und Tierhaltung, des Natur- und Artenschutzes-aber auch der Betriebswirtschaft oder der diversen, für Zoos relevanten rechtlichen Grundlagen und deren Anwendung auskennen. Da sie als Personen in der Öffentlichkeit stehen, haben sie eine grosse gesellschaftliche Verantwortung. Solche Persönlichkeiten zu finden wird im heutigen Umfeld immer schwieriger.
Die Tatsache, dass in den nächsten Jahren einige Zoodirektoren das Rentenalter erreichen und Nachwuchs nicht leicht zu finden ist, zumal es oft an gestaffelten Altersstrukturen im Kader fehlt, hat die Zoos der Alpenregion dazu bewogen, das 6. Rigi-Symposium diesem wichtigen Thema zu widmen. Weil in grösseren Zoos der Direktor viele Aufgaben nicht selbst erledigen kann, sondern sie an die Mitglieder eines Führungsteams delegieren muss, und es zweckdienlich ist, bei einem Direktionswechsel die Führungsstrukturen insgesamt zu hinterfragen, wurden andere Führungspositionen in die Thematik miteinbezogen.
Daraus ist nun ein Leitfaden entstanden, welche Kompetenzen Zookaderleute haben sollen und wie diese erlangt werden können. Die verschiedenen Stellenbeschreibungen im Anhang dienen als Grundlage und können und müssen von jedem Zoo auf seine Bedürfnisse angepasst werden.
Inhalt (Downloads):
| Verfasser | Titel | Downloads Links |
| DOLLINGER, P. | Editorial | HTML |
| - | Teilnehmer | |
| - | Medientext | |
| - | Ergebnisse | |
| CAMENZIND, T. | Wie machen es erfolgreiche Spitäler am Beispiel von Schwyz | |
| STEINER, A. | Wie macht es ein erfolgreiches KMU am Beispiel von Thermoplan | |
| JUNHOLD, J. | Zoodirektor | |
| JANTSCHKE, B. | Zoodirektor | |
| WOLKNER, D. | Kaufmännischer Leiter | |
| RÜBEL, A. | Personalchef | |
| BAUMANN, A. | Marketingleiter | |
| HINDENLANG, K. | Chef Edukation | |
| HECKEL, J.O. | Technischer Leiter | |
| SCHRATTER, D. | Kurator | |
| PAGAN, O, | Zootierarzt | |
| LICHTSTEINER, H. | Potentielle Führungskräfte identifizieren und fördern - Ansätze zur Personalentwicklung in Zoos | |
| MEYER, J. | Ergebnisse der Gruppenarbeit | |
| ANHANG | Stellenbeschreibungen und Pflichtenhefte | |
| ANHANG | Funktionen, Zuständigkeiten - Beispiel | |
| Ganzer Band (mittlere Druckqualität) | PDF |
dollinger-biblio
DOLLINGER, P. (Hrsg., 2012)
Zoos und Reduktion ihres ökologischen Fussabdrucks
Verhandlungsbericht des V. Rigi-Symposiums, gemeinsam organisiert von ZOOSchweiz, OZO und Zoos in Bayern, Goldau-Illgau, 2.-4. Februar 2012. Zoo Office Bern. 86 Seiten.
Editorial:
Bereits im Rahmen des 4. Rigi-Symposiums, das dem Beitrag der Zoos zur Erhaltung der Biodiversität gewidmet war, führte CLAUDE MARTIN, der ehemalige Generaldirektor des WWF International, aus, dass der Biodiversitätsverlust deshalb so massiv ist, weil der ökologische Fussabdruck der anwachsenden Erdbevölkerung immer grösser wird. Der zunehmende Verschleiss von Energie und Materie drohe durch seinen negativen Einfluss auf das Klima die Errungenschaften des Biodiversitätsschutzes zunichte zu machen.
Gerade im Alpenraum werden die Folgen des sich anbahnenden Klimawandels zunehmend manifest: Im Tessin bringen die ursprünglich eingeführten subtropischen Hanfpalmen die heimische Bergwaldvegetation zunehmend durcheinander. Die Ringdrossel verschiebt ihr Areal nach oben und die Amsel rückt nach. Die Gletscher schmelzen und im Gegenzug nehmen Wärme liebende Vogelarten, wie der Bienenfresser oder die Blaumerle im Bestand zu.
Der Betrieb von ganzjährig für das Publikum geöffneten Zoos mit Tieren aller Klimazonen ist sehr energieaufwändig. Ein grösserer Zoo benötigt für seine Tierhäuser, Betriebsgebäude und Publikumseinrichtungen etwa gleich viel Strom, wie 250 Einfamilienhäuser. Um glaubwürdig für Arten- und Umweltschutz sowie nachhaltiges Leben zu werben, fordert daher die WELT-ZOO- UND AQUARIUM-NATURSCHUTZ-STRATEGIE von den Zoos, Anstrengungen zu unternehmen, um die von ihnen produzierten CO2-Mengen - und damit ihre Mitverantwortung für den Klimawandel und die daraus resultierende Lebensraumzerstörung - zu minimieren.
Unter diesen Gesichtspunkten beschlossen die Veranstalter das 5. Rigi-Symposium dem Thema „Wie können Zoos ihren ökologischen Fussabdruck reduzieren?“ zu widmen.
Das Symposium fand diesmal nicht auf der Rigi selbst statt, sondern an einem vergleichbar abgeschiedenen Ort in der Region, womit die spezielle Ambiance dieser Klausurtagung gewahrt werden konnte. Der Ablauf folgte jedoch dem bewährten Muster: Allgemeine Vorträge führten in das Thema ein, so referierte ULRICH GROBER zur Theorie und Geschichte der Nachhaltigkeit, eines Begriffs, der bereits im 18. Jahrhundert geprägt wurde, der aber erst in jüngster Zeit von der Forstterminologie in den allgemeinen Sprachschatz übergegangen ist, und BERT BEYERS erklärte den Ansatz des Global Footprint Network. Seine Aussage, dass man nur managen kann, was man auch messen kann, wurde durch die nachfolgenden Vorträge, die sich mit konkreten Beispielen auseinandersetzten, bestätigt. GERALD DICK schliesslich verwies auf die WELT-ZOO- UND AQUARIUM-NATURSCHUTZSTRATEGIE als strategischen Überbau für Massnahmen zur Reduktion des ökologischen Fussabdrucks der Zoos.
Als Musterbeispiele aus anderen Branchen präsentierte ISABEL SPECKER, wie bei der Migros mit dem Thema Nachhaltigkeit umgegangen wird, KATHARINA TEUSCHER stellte die Umwelt Arena Spreitenbach vor, eine Ausstellungs- und Eventplattform, die das Publikum für nachhaltiges Handeln sensibilisieren will, und MICHAELA REITTERER berichtete von ihren Erfahrungen mit dem Umbau des Boutique Hotels Stadthalle in Wien zum weltweit ersten Null-Energie-Bilanz Hotel im urbanen Raum.
Schliesslich wurde anhand von acht Beispielen dargelegt, was einzelne Zoos für Nachhaltigkeitsstrategien entwickelt und was sie konkret unternommen haben, um diese umzusetzen.
Bei den Diskussionen am Samstag zeigten sich die Teilnehmer darin einig, dass jeder Zoo zur Verringerung seines ökologischen Fussabdrucks beitragen und dies auch dokumentieren soll. Man war sich auch einig darin, dass die in diesem Zusammenhang notwendige Datenerfassung nicht für ein Benchmarking zwischen den Zoos verwendet werden kann, da in jeder Einrichtung die Voraussetzungen andere sind, sondern dass sie ausschliesslich dem langfristigen Monitoring im eigenen Betrieb dienen soll. Nicht einig war man sich in der Frage, ob der Energieverbrauch der anreisenden Besucher bei Berechnungen zu berücksichtigen sei, da der Zoo diesbezüglich kaum Einflussmöglichkeiten hat.
| Verfasser | Titel | Downloads Links |
| DOLLINGER, P. | Editorial | HTML |
| - | Teilnehmer | |
| - | Medientext | |
| - | Ergebnisse | |
| BIJLEVELD, C. | Kompensationsfonds der Zoos und Aquarien | |
| GROBER, U | Zur Theorie und Geschichte der Bachhaltigkeit | |
| BEYERS, B. | Der Ansatz des Global Footprint Network | |
| DICK, G. | Ökologischer Fussabdruck und Nachhaltigkeit: mögliche Beiträge der Zoos | |
| SPECKER, I. | Nachhaltigkeit bei der Migros | |
| TEUSCHER, K. | Modern bewusst leben - Die erste Umweltarena der Welt | |
| REITTERER, M. | Das Boutique-Hotel Stadthalle in Wien | |
| JUNHOLD, J. | Die Dimensionen der Nachhaltigkeit in der Tropenerlebniswelt Gondwanaland | |
| CLEMENTS, A. | Gelebte Nachhaltigkeit im Zoo Zürich | |
| HECKEL, J.-O. | Klimaschutz und Nachhaltigkeit - Wo steht der Zoo Landau | |
| BIJLEVELD, C. | Beispiel Papiliorama Kerzers | |
| SCHÖNBÄCHLER, T. | Ressourcenbedürfnisse und -optimierung im Zoo Basel | |
| HANNEHEN, F. | Energiekonzept im Zoo Osnabrück | |
| STAUFFER, C. | Mobilitätsstrategie als Kernelement derNachhaltigkeitsstrategie im Wildnispark Zürich | |
| BERLING, T. | Regionalität als Massstab für Nachhaltigkeit | |
| CLEMENTS, A. | Auswertung Fragebogen | |
| BIEK, K. | Erhebungsbogen für CO2-Footprint | |
| VOLLAND, B. et al. | Nachhaltige Stadt Zürich | |
Literatur:
MARTIN, C. (2010): Situation der Biodiversität weltweit. Verh. Ber. 4. Rigi-Symposium: 24-26.
SCHMID, H. ET AL. (2001): Die Entwicklung der Vogelwelt in der Schweiz. Avifauna Report Sempach 1, Annex. 444 Seiten.
WAZA (2005): Zoos und Aquarien für Naturschutz. Die Welt-Zoo- und Aquarium-Naturschutzstrategie. WAZA Geschäftsstelle, Bern. ISBN 3-033-428-8.
dollinger-biblio
Gebirge (4): Hochgebirge in Zentralasien
![]()
Allgemeines
|
|
Auf diesem Datenblatt werden eurasische Gebirge östlich des Urals vorgestellt. Die Gebirge Zentralasiens sind aufgrund ihrer Topografie und ihres extremen Klimas von besonderem Interesse. Der Altai hat eine vielfältige Fauna, weil er die sibirische Taiga mit der mongolischen Wüste verbindet. Die Berge Süd-Zentral-Chinas sind ein Brennpunkt der Biodiversität. Alle drei Gebiete beherbergen zahlreiche Tierarten, die in Zoos gehalten werden. Typische Zootiere
Schneehase, Luchs, Manul, Schneeleopard, Wolf, Rothund, Rotfuchs, Kragenbär, Kleiner Panda, Buntmarder, Kiang, Sibirisches Moschustier, Maral, Weisslippenhirsch, Hausyak, Sibirischer Steinbock, Markhor, Argali, Blauschaf, Himalaya-Tahr, Takin. Rostgans, Streifengans, Steinadler, Kaiseradler, Bartgeier, Schneegeier, Turmfalke, Königsglanzfasan, Weißer Ohrfasan, Satyrtragopan, Sibirischer Uhu, Habichtskauz, Kolkrabe, Alpenkrähe. |
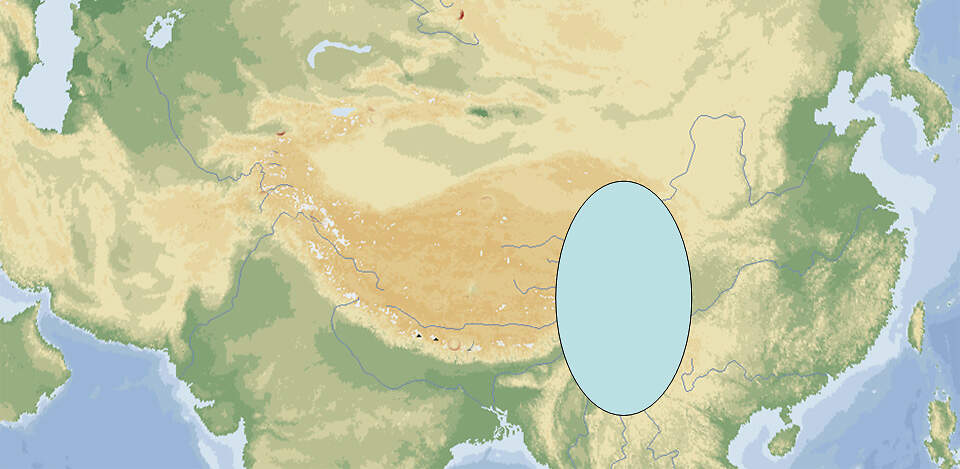
Zentralasiens Hochgebirge rund um Tibet
|
|
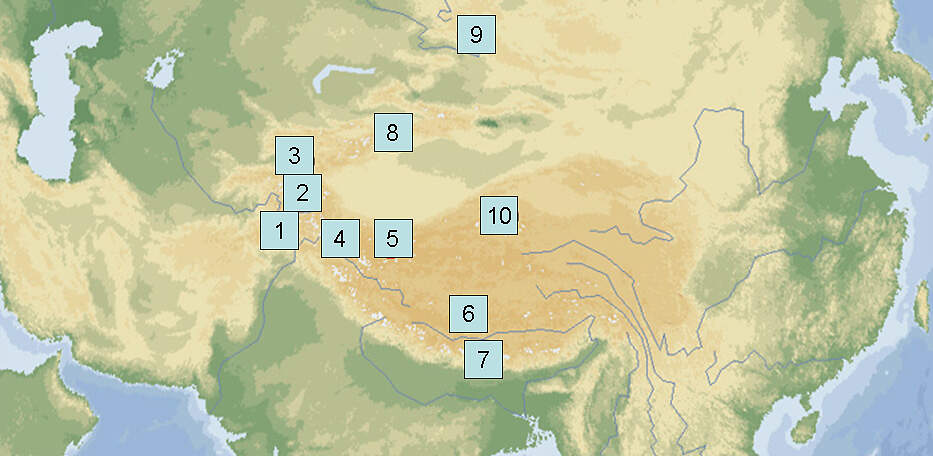
Die aus Gebirgsketten, Gebirgsmassiven und Hochplateaus bestehende zentralasiatischen Hochgebirgsregion liegt zu einem guten Teil auf über 3'000 m.ü.M., mit 14 Achttausenden als höchsten Erhebungen. Wie die tertiären Faltengebirge Europas verlaufen die Ketten im Wesentlichen in west-östlicher Richtung und biegen erst im Osten nach Norden oder Süden ab. Wichtige Gebirge sind (höchster Berg): Hindukusch (Tirich Mir, 7'708 m), Pamir (Kongur Tagh, 7'649 m), Alai (Pik Tandykul, 5'544 m), Himalaya (Mount Everest, 8'848 m), Transhimalaya (Nyainqêntanglha, 7'162 m), Tienschan (Dschengisch Tschokusu, 7'439 m), Kunlun (Liushi Shan, 7167 m), NanShan (Shule Shan, 6'346 m), Karakorum (K2, 8'611 m), Altai (Belucha, 4'506 m) und das Große Schneegebirge Sichuans (Minya Konka, 7556 m). Eingerahmt von Pamir, Karakorum, Transhimalaya, Kunlun- und NanShan-Gebirge sowie den Bergen von Sichuan liegt auf 4000-4500 m Höhe das Hochland von Tibet mit einer Fläche von und 2 Millionen km². Es ist eine kalte Hochgebirgswüste charakterisiert durch großflächige Ebenen mit spärlicher Vegetation, Senken mit Seen oder sumpfigen Talböden, vegetationslosen Schotterböden und versalzten Zonen (DENZAU, 1999). Das Klima im Zentrum der Region ist extrem kontinental, sehr trocken und mit Temperaturen von -60 bis +40°C. In den Randgebirgen fallen dagegen reichlich Niederschläge, die letztlich in das Polarmeer bzw. den Indopazifik mit seinen Nebenmeeren fließen oder durch Syr-Darja und Amu-Darja dem Aralsee zugeführt werden. Vegetation und CharakterpflanzenIn den niederschlagsarmen Teilen der Region Hochsteppen, Halbwüsten, kalte Gebirgswüsten. Charakterpflanzen sind hier Gräser der Gattungen Stipa, Poa, Elymus, Seggen (Carex, Kobresia), Salzkräuter (Salsola), Astern, Beifuß (Artemisia), Hornmelde (Krascheninnikovia), Tragant (Astragalus), und und Erbsensträucher (Caragana) (DENZAU, 1999). An der Peripherie je nach Entfernung vom Meer und Exposition unterschiedliche Pflanzengesellschaften, einschließlich Laub- und Koniferenwälder. TierweltZentralasiatischer Luchs, Manul, Schneeleopard, Wolf, Rothund, Rotfuchs, Tibetfuchs (Vulpes ferrilata), Tibet- und Himalaya-Braunbär, Kragenbär, Kiang, Südchinesische Rothirsche, Weisslippenhirsch, Wild- und Hausyak, Tibetgazelle (Procapra picticauda), Tibetantilope (Pantholops hodgsoni), Sibirischer Steinbock, Markhor, Argali, Blauschaf, Himalaya-Tahr, Himalaya-Serau (Capricornis tahr), Himalaya-Goral (Naemorhedus goral), Tibetanischer Wollhase (Lepus oiostolus), Schwarzlippen- und weitere Pfeifhasenarten, Langschwanz- (Marmota caudata), Himalaya- (M. himalayana) und Menzbiers Murmeltier (M. menzbieri), Ornithologisch bedeutende Gebiete (u.a. Hemis-Nationalpark, IN-007, Khunjrab-Nationalpark, PK001, Klein-Pamir, AF-004, Mount Tuomuer-Nationalpark, CN121, Changtan-Plateau, CN132): Rostgans, Streifengans, Steinadler, Kaiseradler, Bartgeier, Schneegeier, Turmfalke, Himalaja- und Tibet-Königshuhn (Tetraogallus himalayensis, T. tibetanus), Tibet-Rebhuhn (Perdix hodgsoniae), Königsglanzfasan, Weißer Ohrfasan, Satyrtragopan, Mauerläufer, Kolkrabe, Alpenkrähe, Schneefinken (Montifringilla spp.) ... |
Literatur und Internetquellen
- BIRDLIFE DATA ZONE
- CHAPMAN, J. A. & FLUX, J. E. C. (1990)
- DENZAU, G. & H. (1999)
- PFEFFER, P. (1969)
- SHACKLETON, D.M. (1997)
Altai
|
|
Der Altai ist ein 2100 km langes, nördlich der Wüste Gobi gelegenes Gebirge im Grenzgebiet von Kasachstan, Russland, der Mongolei und China, das in die Teilgebirge Russischer, Mongolischer und Gobi-Altai unterteilt wird. Es ist „nur“ etwa so hoch wie die Alpen. Der höchste Berg ist die im Russischen Altai gelegene Gora Belucha (4506 m). Zwischen den Bergketten liegen in Höhenlagen von 1000 bis 1800 m Ebenen als Relikte glazialer Seen, z.B. das Uimonbecken. Auf 2000 bis 3000 m befinden sich Hochplateaus, wie z.B. die Ukok-Hochfläche. Mit langen, kalten Wintern und kurzen, bisweilen recht heißen Sommern ist das Klima des Altai stark kontinental geprägt. Die Niederschlagsmengen variieren regional beträchtlich. Die westlichen und nördlichen Teile des Russischen Altai erhalten die höchsten Niederschläge, in Gipfellagen bis 1500 mm. Die südlichen Teile, insbesondere der Gobi-Altai, sind mit einer jährlichen Niederschlagsmenge bis zu 300 mm viel trockener. Vegetation und CharakterpflanzenIn tiefen und mittleren Lagen des Südens Steppenvegetation. Wald ab 350 m oder höher bis 2400 m. Im Norden fließender Übergang von der Taiga in subalpine Waldvegetation bis auf etwa 1500-1800 m. Die Wälder und Waldsteppen des Altai setzen sich im Wesentlichen zusammen aus kleinblättrigen Laubbäumen wie Hängebirke (Betula pendula), Eberesche (Sorbus sibirica), Traubenkirsche (Padus racemosa) und Espe (Populus tremula) sowie Koniferen, wie Sibirische Fichte (Picea obovata), Sibirische Tanne (Abies sibirica), Sibirische Lärche (Larix sibirica), Sibirische Zirbelkiefer (Pinus sibirica) und, auf Sandböden, Wald-Kiefer (Pinus sylvestris). Darüber bis zur Schneegrenze, die auf 2400 bis 3000 m liegt, Waldtundren mit Zwergbirken (Betula nana), Heckenkirschen (Lonicera hispida), Zwergmispeln (Cotoneaster uniflorus) und Johannisbeeren (Ribes), alpines Grasland oder Moore und, auf den Hochplateaus, Gebirgstundren mit Moosen und Flechten. Die bis über 4000 m hohen Gipfel sind mit Firn bzw. Gletschern bedeckt, wobei die Gletscher eine Ausdehnung von gegen 900 km² haben. TierweltDie Fauna des Altai unterscheidet sich von jener der Gebirge rund um Tibet dadurch, dass sie Elemente der subarktischen Taiga enthält. Altai-(Zentralasiatischer) Luchs, Manul, Schneeleopard, früher auch Sibirischer Tiger, Wolf, Rothund, Rotfuchs, Steppenfuchs, Vielfrass, Zobel (Martes zibellina), Steinmarder, Feuerwiesel, Altaiwiesel (Mustela altaica), Hermelin, Mauswiesel (Mustela nivalis), Dachs, Fischotter, Sibirischer Braunbär, Wildschwein, Sibirisches Moschustier, Maral, Elch, Sibirisches Waldrentier (R. t. valentinae), und Sibirisches (Asiatisches) Reh, ehemals Wisent, Sibirischer Steinbock, Argali. An Kleinsäugern findet man u.a. Schneehase, Altai-Pfeifhase (Ochotona alpina), Graues (Marmota baibacina) und Sibirisches (M. sibirica) Murmeltier. Ornithologisch bedeutendes Gebiete (CN092) mit u. a. Altai-Königshuhn (Tetraogallus altaicus), Felsen-Auerhuhn (Tetrao parvirostris), Sibirischem Uhu und Habichtskauz. |
Literatur und Internetquellen
- BIRDLIFE DATA ZONE
- BIBIKOV, D. I. (1968)
- CHAPMAN, J.A. & FLUX, J.E.C. (1990)
- PFEFFER, P. (1969)
- SHACKLETON, D.M. (1997)
Berge Süd-Zentral-Chinas
|
|
Das als Brennpunkt der Biodiversität definierte Gebiet umfasste ursprünglich 800'000 km². Davon sind nur 64'000 km² noch einigermaßen intakt und nur 26'562 km² stehen unter Schutz. Die Artenvielfalt umfasst ca. 12'000 Gefäßpflanzen, wovon ca, 3'500 endemisch sind, 686 Arten Vögel (36 Endemiten), 300 Säugetiere (36), 70 Reptilien (16) und 84 Amphibien (51). Vegetation und CharakterpflanzenBambuswälder, rund 230 Arten Rhododendren. Endemische Koniferenarten sind der Urweltmammutbaum (Metasequoia glyptostroboides) und der Taubenbaum (Cathaya argyrophylla). TierweltStumpfnasenaffen (Rhinopithecus), Eurasischer Luchs, Nebelparder, Schneeleopard, Leopard, Tiger, Wolf, Rothund, Riesenpanda, Kragenbär, Kleiner Panda, Buntmarder, Chinesisches Moschustier (Moschus berezowskii), Schopfhirsch, Weißlippenhirsch, Sambar, Takin, Chinesische Serau (Capricornis milneedwardsii), Roter Goral (Naemorhedus baileyi). Ornithologisch bedeutende Gebiete (u.a. Baishui Jiang-Naturschutzgebiet, CN169), Wolong-Naturschutzgebiet, CN201, Gongga Shan-Naturschutzgebiet, CN219, Wulianfeng, CN266): Bindenseeadler (Haliaeetus leucoryphus), Goldfasan, Amherstfasan, Blauer und Weißer Ohrfasan, Grünschwanz-Glanzfasan (Lophophorus lhuysii), Humefasan (Syrmaticus humiae), Blutfasan (Ithaginis cruentus), Temminck- und Blyth-Tragopan (Tragopan blythii), Schwarzhalskranich, Kansuhäherling (Garrulax sukatschewi). |
Literatur und Internetquellen
- BIRDLIFE DATA ZONE
- MITTERMEIER, R.A., MYERS, N. & GOETTSCH-MITTERMEIER, C. (1999)
- PFEFFER, P. (1969)
Zurück zu Lebensräume in Eurasien
Weiter zu Mittelmeeraum
Dickicht
|
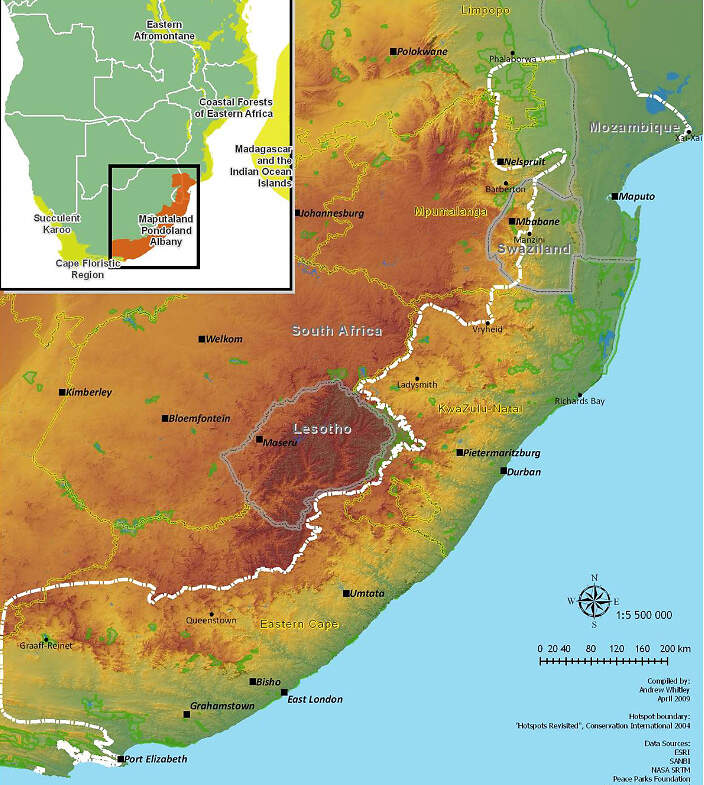
(4.5) Allgemeines (4.5.2) Albany-Buschland und -Dickicht ------------------------------------------------------------------- ------------------- ---- |
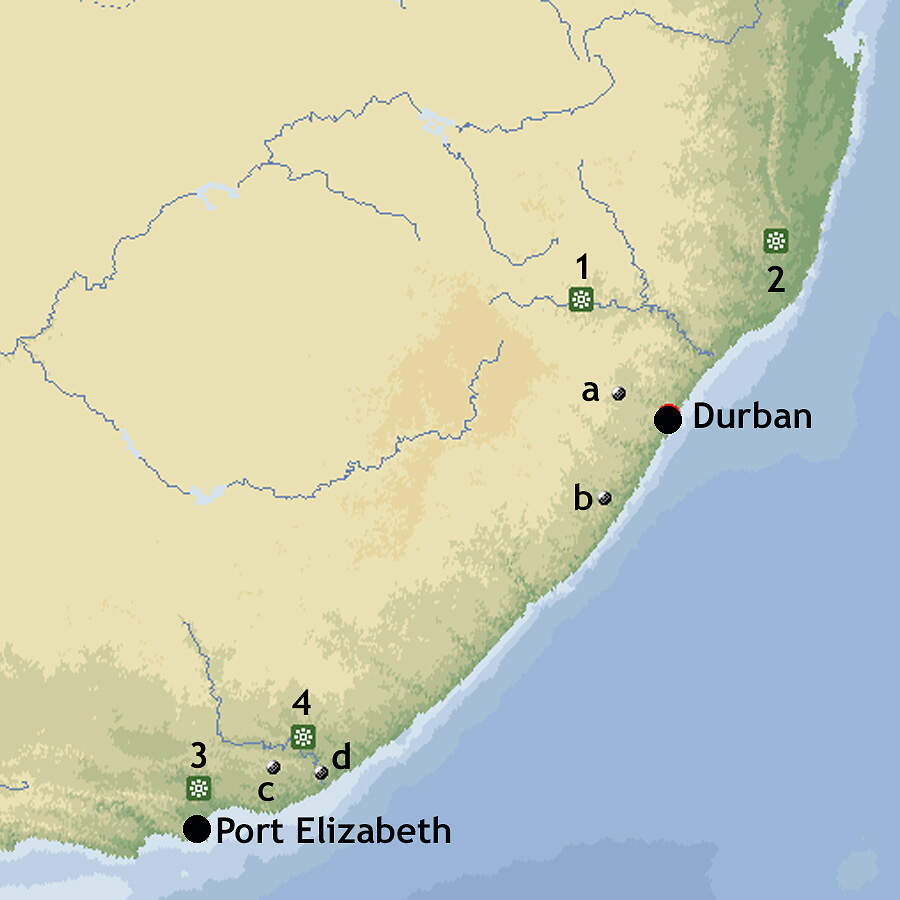 (1) Weenen-NR, (2) Hluhluwe-iMfolozi-Park, (3) Addo-Elefanten-NP, (4) Great Fish River-NR. (a) Queen-Elizabeth-NP, (b) Oribi-Gorge-NR, (c) Thomas-Baines-NR , (d) Waters-Meting-NR |
Allgemeines
|
Die auf Englisch "Thicket" genannte, natürlicherweise fragmentierte Ökoregion liegt zwischen den Drakensbergen und dem Küstenwald. Sie reicht vom Ostkap bis in den Süden Mpumalangas und Mosambiks und bildet ein Mosaik mit Savanne und anderen Vegetationstypen. Das als Brennpunkt der Biodiversität definierte Gebiet umfasst 274'138 km². Davon sind rund 24 % noch intakt und etwa 8 % stehen unter Schutz. Die Biodiversität ist sehr hoch. Es sind 8'100 Gefäßpflanzen, 1'016 terrestrische Wirbeltierarten und 73 Fischarten bekannt. 1'900 Pflanzenarten, 45 terrestrische Wirbeltierarten und 20 Fischarten sind endemisch. Dickicht kommt auch außerhalb der definierten Ökoregion in Fynbos, Sukkulenter und Nama-Karoo, sowie Savanne und Trockenwald vor. Literatur und Internetquellen
|
Maputaland-Pondoland-Buschland und -Dickicht
Nationalparks und andere Schutzgebiete
Weenen-Naturschutzgebiet
|
|
Bestehend seit 1974. Vollständig eingezäunte Fläche von 4'908 ha. Das Schutzgebiet ist Teil des 60'000 ha umfassenden Thukela-Biosphären-Reservats. Es liegt auf 898-1306 m Höhe. Jahresniederschlag (Weenen Dorp) ca. 660 mm. Vegetation: Dickicht mit Afrikanischem Ölbaum (Olea europaea subsp. africana), Rotem Elfenbeinholz (Berchemia zeyheri), Bergkohlbaum (Cussonia paniculata), Kandelaber-Euphorbie (Euphorbia candelabrum) und der seltenen Grasaloe (Aloe spectabilis) namentlich im Tal des Bushman's River, ansonsten Akaziensavannen und Grasland. Zu den häufigen Baumarten gehören Acacia karoo, A. nilotica, A. robusta, A. sieberiana, A. tortilis, Witgat (Boscia albitrunca), Ficus-Arten, Flaschenbürstenstrauch (Greyia sutherlandii). Tierwelt: Seit Beginn vorhanden oder spontan eingewandert sind Schabrackenschakal, Kap-Fingerotter, Tüpfelhyäne, Braune Hyäne, Erdwolf, Serval, Leopard, Erdferkel, Buschschwein (Potamochoerus larvatus), Buschbock, Bergriedbock, Steinböckchen und Klippspringer. Wiederangesiedelt wurden Breit- und Spitzmaulnashorn, Steppenzebra, Kapgiraffe, Kaffernbüffel, Elenantilope, Großer Kudu, Pferdeantilope, Südafrikanische Kuhantilope, Bergriedbock , Großriedbock (Redunca arundinum), Südafrikanischer Strauß. Die Avifauna umfasst über 250 Arten. Während des Sommers sind z. B. 8 Kuckucksarten anzutreffen: Schwarz-, Afrikanischer, Einsiedlerkuckuck (Cuculus clamosus, C. gularis, C. solitarius), Häher-, Jakobiner-, Kapkuckuck (Clamator glandarius, C. jacobinus C. levaillantii), Gold- und Klaaskuckuck (Chrysococcyx caprius, C. klaas). Ferner sind besonders beachtenswert Namaspecht (Thripias namaquus), Weißkehlrötel (Cossypha humeralis), Meisensänger (Parisoma subcaeruleum), Angolagirlitz (Serinus albogularis) und Rotkopfamadine (Amadina erythrocephala). An großen Vögeln gibt es Schwarzstörche, die vermutlich auf Felsen in de Schlucht des Bushmans River brüten, Sekretäre und Paradieskraniche. Literatur und Internetquellen |
Hluhluwe-iMfolozi-Park
|
|
Die Schutzgebiete von Hluhluwe und Umfolozi (offizielle Schreibweise heute: iMfolozi) wurden am 27. April 1897 (nach anderen Quellen am 30. April 1895) offiziell gegründet. Sie haben eine Fläche von 23'067 bzw. 47'753 ha. 1989 wurden sie durch einen Korridor verbunden, wodurch der 96'453 ha große, vollständig eingezäunte Hluluwe-iMfolozi-Park entstand. Das Terrain ist hügelig, Höhenlagen von 90-586 m.ü.M. Der Jahresniederschlag beträgt etwa 600 mm im Süden von Umfolozi bis 1250 mm beim Hilltop Camp im Norden von Hluhluwe. Die höchsten Niederschläge fallen von Februar bis April. Die mittlerer Tiefsttemperatur wird im Juli mit 12°C erreicht, die mittlere Höchsttemperatur im Dezember mit 30.5°C. In Umfolozi können die Tagestemperaturen bis auf 38°C steigen. Vegetation: Die Vegetation des Parks ist äußerst vielfältig, wobei relativ wenig endemische Arten vorkommen. Sie umfasst Dickicht und Busch mit Kalahari-Weihnachtsbaum (Dichrostachys cinerea) and Akazien, lockere Savanne mit Schirmakazien (A. tortilis), Trockenwälder mit Marulabäumen (Sclerocarya birrea) und Süßdornakazien (A. nigrescens), Grasland (Northern Zululand Sourveld) und Galeriewald mit Sykomoren (Ficus sycomorus) und Afrikanischem Ebenholz (Diospyros mespiliformis) (SCOTT-SHAW & ESCOTT, 2011, unpubl.). Der Name Hluhluwe leitet sind von einer dornigen Liane (Dalbergia armata) ab, die auf isiZulu "umHluhluwe" genannt wird. 20 invasive Pflanzenarten gefährden die einheimische Vegetation. Am problematischsten sind Siamkraut (Chromolaena odorata) und Zedrachbaum (Melia azedarach ) (MACDONALD, 1983). Tierwelt: Die Parks wurden ursprünglich eingerichtet, um das Breitmaulnashorn vor dem Aussterben zu bewahren, was ein voller Erfolg war. Nebst dem Breitmaul- mit 1'500 ist auch das Spitzmaulnashorn mit 360 Individuen gut vertreten, ferner leben hier u.a. Grüne Meerkatze, Weisskehlmeerkatze, Bärenpavian, Schabrackenschakal, Serval, Leopard, Tüpfel- und Braune Hyäne, Zuluzebra, Flusspferd, Warzenschwein, Buschschwein (Potamochoerus larvatus), Kaffernbüffel, Elenantilope, Großer Kudu, Tiefland-Nyala, Buschbock, Rotducker, Kronenducker, Streifengnu, Wasserbock , Bergriedbock, Großriedbock (Redunca arundinum), Impala (23'000 Stück!), Steinböckchen und Klippspringer. Wiederangesiedelt wurden Afrikanischer Wildhund, Löwe, Gepard, Kapgiraffe, Rotschnabel-Madenhacker und zwischen 1985 und 1991 etwa 160 Elefanten. Die Wiederansiedlung der Elefanten hatte zum Ziel, der Verwaldung es Parks entgegen zu wirken. Der Park ist ein ornithologisch bedeutendes Gebiet (IBA ZA046) mit über 425 Arten, darunter Kahlkopfrapp, Kapgeier (Gyps coprotheres), Weißrückengeier, Wollkopfgeier,Ohrengeier, Palmgeier, Raubadler, Kampfadler, Gaukler, Graubrustschlangenadler (Circaetus fasciolatus), Sekretär, Wachtelkönig (Wintergast), Kaptriel, Braunkopfpapagei (Poicephalus cryptoxanthus), etwa 30 Südliche Hornraben, Trompeterhornvogel und drei Tockus-Arten, drei Arten Frankoline, Kräuselhauben- und Helmperlhuhn, drei Arten Turakos, acht Arten Kuckucke und zehn Arten Eulen. Die Herpetofauna schliesst ua mit ein: Nilkrokodil , Glattrand-Gelenkschildkröte , Pantherschildkröte, Starrbrust-Pelomeduse (Pelomedusa subrufa), Felsagame (Agama atra), Lappenchamäleon (Chamaeleo dilepis), Riesenskink (Acontias plumbeus), Delalande-Sandveldeidechse (Nucras lalandii), Afrikanische Strauchnatter (Philothamnus semivariegatus), Östliche Tigerschlange (Telescopus semiannulatus), Kap-Vogelnatter (Thelotornis capensis), Afrikanische Eierschlange, Puffotter , Rauten-Krötenviper (Causus rhombeatus). Literatur und Internetquellen
|
![]()
Weitere Parks mit Maputaland-Pondoland-Buschland und -Dickicht
(Die Liste erhebt keinen Anspruch auf Vollständigkeit)
|
Kwazulu-Natal: Mhlopeni-Naturschutzgebiet, Oribi-Gorge-Naturschutzgebiet, Queen-Elizabthe-Nationalpark, Ubizane-Wildschutzgebiet |
Albany-Buschland und -Dickicht
Addo-Elefanten-Nationalpark
|
|
Gegründet am 03.07.1931 auf eine Fläche von erwa 4'000 ha. Sukzessive Vergrößerung, bis 1991 auf 11'718 ha, bis 1996 Integration des Zuurberg Nationalparks und Expansion auf 54'000 ha, wovon 12'126 ha für die Elefanten zur Verfügung standen. Danach Integration und weitere Expansion auf heute 170'000 ha. Die nachfolgenden Informationen beziehen sich nur auf das Kerngebiet, da in de Zuurberg-, Darlington-Damm und Alexandria Forest-Sektion völlig andere Vegetationstypen vorherrschen: Nicht-nachhaltige Bejagung für im 19. Jahrhundert zu einer Beinahe-Ausrottung des Elefanten in Südafrika. In der östlichen Kapprovinz überlebte, nebst einigen Tieren im Knysna-Wald, eine einzige Herde, bei der die Bullen nur bescheidene, die Kühe meist gar keine Stosszähne trugen. Diese Herde hatte sich in die mit dichtem Speckbaumdickicht bestandenen Hügel um die Ortschaft Addo zurückgezogen, die wegen Wassermangels landwirtschaftlich nicht genutzt werden konnte. Die Hügel waren aber rundum von Ackerbaubetrieben und Obstplantagen umgeben, und die Elefanten gerieten wegen der Landschäden, die sie verursachten, immer wieder in Konflikt mit den Farmern. 1919 wurde beschlossen, die Elefanten auszurotten. In den folgenden Jahren wurden 120 Tiere abgeschossen, bis sich das öffentliche Gewissen regte. 1931 wurde ein Gebiet als Addo Elephant National Park ausgeschieden und die restlichen Elefanten hineingetrieben. Es waren noch elf Stück. Unter dem Schutz des Parks vermehrte sich die Herde, anfänglich allerdings sehr langsam. 1954 umfasste sie erst 18 Tiere. Konflikte mit den Farmern waren nach wie vor an der Tagesordnung. Man versuchte sie zu umgehen durch Ablenkfütterungen mit Orangen. 1954 wurde ein elefantensicherer Zaun um einen zuerst 22, später etwa 50 km2 grossen Teil des Parks gelegt, womit das Problem vorerst geregelt war. Das Resultat war zwar etwas, was sich von einer Zoohaltung fast nur noch durch die Dimension unterschied, aber immerhin hatten die Elefanten die Möglichkeit, sich ungestört zu vermehren, was sie auch fleissig taten: nach zehn Jahren betrug der Bestand 43 Tiere, nach 20 Jahren waren es 75 und 1984 bereits 118. 1991 gelang es, den Addo Elephant National Park auf 117 km2 zu erweitern. Damit konnte Platz für maximal 220 Elefanten geschaffen werden. 1994 wurde aber bereits die 200er Marke erreicht, was weitere Vergrößerungen des Elefantenarereal erforderlich machte. Für 2014 wird der Bestand mit 620 angegeben. Heute werden die Elefantekühe zum Teil unter Hormone gesetzt, um das Populationswachstum zu bremsen. Zur Erhöhung der genetischen Bandbreite wurden Elefantenbullen aus dem Kruger-Nationalpark einegführt. Vegetation und Charakterpflanzen: Mehr als 90 % der Fläche wird vom Spekboomveld eingenommen, einem der fünf Subtypen des Albany-Dickichts. Charakterpflanze ist der sukkulente Speckbaum (Spekboom, Portulacaria afra). Dieser bildet die hauptsächliche Nahrungsgrundlage der Elefanten, der Büffel und verschiedener Antilopen. Außerhalb des Parks ist er sehr selten geworden. Ferner kommen u.a. Karoo-Burenbohne (Schotia afra, ein Johannisbrotgewächs), zwei Sumachbaum-Arten (Rhus longispina und tomentosa ), Amathungulu-Busch oder Num-num (Carissa macrocarpa ), Nadelbusch (Azima tetracantha ) und Ghwarrie-Busch (Euclea undulata ), Uitenhage-Aloe (Aloe africana ) und mehrere Euphorbienarten vor. Tierwelt: Als größere Säuger hatten im Gebiet des ursprünglichen Parks Grüne Meerkatze, Schabrackenschakal, Karakal, Erdferkel, Elefant, Buschschwein (Potamochoerus larvatus), Kaffernbüffel, Großer Kudu, Buschbock, Kronenducker, Kap-Greisbock und Weißschwanz-Stachelschwein überlebt. Löwe, Tüpfelhyäne, Elenantilope, Südafrikanische Kuhantilope, Großriedbock (Redunca arundinum) und Bergriedbock wurden (wieder-)angesiedelt. Die in den 1960er Jahren angesiedelten Ostafrikanischen Spitzmaulnashörner (D. b. michaeli) wurden nach 1990 durch Tiere der südlichen Unterart (D. b. bicornis) aus Namibia ersetzt. Heute zählt der Park im "Main Camp and Game Area" 47 Säugetierarten ohne Fledermäuse 253 Vogel-, 54 Reptilien- und 19 Amphibienarten. In allen Sektionen des Parks wurdenj 417 Vogelarten Besonders bemerkenswert ist der flugunfähige Riesenpillendreher, der nach der Ausrottung von Elefant und Nashorn außerhalb des Parks fast überall ausstarb. Literatur und Internetquellen |
Great Fish River-Naturschutzgebiet
|
|
Das Great Fish River-Naturschutzgebiet entstand durch den Zusammenschluss der früheren Andries Vosloo- und Sam Knott- Schutzgebiete der alten Kapprovinz und des Double Drift-Wildschutzgebiet des ehemaligen Homelands Ciskei. Es umfasst rund 45'000 ha. Benachbart befindet sich das private Kwandwe-Naturschutzgebiet mit 22'000 ha. Die höchsten Hügel sind etwas über 500 m hoch. Vegetation und Charakterpflanzen: Klassifiziert als Fish River Valley Bushveld und charakterisiert durch etwa 2 m hohe dornige Gehölze, Euphorbien und Aloen. Die Wiederansiedling des Spitzmaulnashorns und anderer Herbivoren sowie die Zunahme der Pavianbestände haben zu einem deutlichen Rückgang von Euphorbien-Arten (Euphorbia bothae, E. tetragona and E. triangularis) geführt (LENT et al., 2009; LUSKEL et al. (2009). Tierwelt: Ursprünglich eingerichtet zum Schutz des Großen Kudus. Zusätzlich zu den noch autochthon vorkommenden Tierarten, wie Grüne Meerkatze, Bärenpavian (Papio ursinus), Schabrackenschakal, Kap-Fingerotter, Tüpfelhyäne, Karakal, Leopard, Buschbock, Kronenducker, Steinböckchen und Springbock wurden zahlreiche weitere wiederangesiedelt, so Spitzmaulnashorn, Steppenzebra, Flusspferd, Warzenschwein, Kapgiraffe, Kaffernbüffel, Elenantilope, Südafrikanische Kuhantilope, Streifengnu, Blessbock und Impala. Der Park ist nicht auf der Liste der ornithologisch wichtigen Gebiete, es kommen aber mindestens 245 Vogelarten vor, im benachbarten Kwandwe-Reserbat wurden deren 302 nachgewiesen. Pantherschildkröten sind häufig anzutreffen, Afrikanische Felsenpythons wurden (Python sebae) wurden wiederangesiedelt. Literatur und Internetquellen |
![]()
Weitere Parks mit Albany-Buschland und -Dickicht
(Die Liste erhebt keinen Anspruch auf Vollständigkeit)
|
Ost-Kap: Blaauwkrantz-NaturschutzgebietKariega-Wildpark, Karringmelkspruit-Naturschutzgebiet, King-Williams-Town-Naturschutzgebiet, Kowie-Naturschutzgebiet, Mpofu-NaturschutzgebietMpongo-Park, Thomas-Baines-Naturschutzgebiet, Waters-Meeting-Naturschutzgebiet |
![]()
Zurück zu Übersicht Südliches Afrika
Weiter zu Trockensavannen und Grasländer
ZIEGLER, T., OHLER, A.; THANH, Vu Ngoc ; QUYET, Le Khac ; THUAN, Nguyen Xuan; TRI, Dinh Hu (2006)
Review of the amphibian and reptile diversity of Phong Nha – Ke Bang National Park and adjacent areas, central Truong Son, Vietnam.
Herpetologica Bonnensis, II: 247-262.
Abstract:
The authors provide an updated review of the herpetofauna of the Phong Nha-Ke Bang National Park including adjacent areas within the Quang Binh province, central Vietnam. Beside confirmation of species and specific allocation of previously undetermined taxa, we herein add 19 species (2 Megophryidae, 1 Dicroglossidae, 2 Ranidae, 2 Rhacophoridae, 2 Geoemydidae, 1 Gekkonidae, 1 Lacertidae, 1 Scincidae, and 7 Colubridae) which were not known from the region before. For each of these we provide information about distribution, natural history and characteristic features. Meanwhile, 140 amphibian and reptile species are known from the karst forests of the Phong Nha-Ke Bang National Park, representing more than 30 percent of the herpetofauna currently known for the country.
RAMBERG, L., HANCOCK, P., LINDHOLM, M., MEYER, T., RINGROSE, S. , SLIVA, J., VAN AS, J. & VA
Species diversity of the Okavango Delta, Botswana.
Aquat. Sci. 68 (2006) 310–337. ISSN 1015-1621/06/030310-28. DOI 10.1007/s00027-006-0857-y © Eawag, Dübendorf, 2006
Abstract:
In the Okavango Delta (about 28,000km2) the number of identified species is 1,300 for plants, 71 for fish, 33 for amphibians, 64 for reptiles, 444 for birds, and 122 for mammals. The local occurrence of different species of these taxonomic groups in the Okavango Delta is mainly due to a hydrological gradient from permanent streams and swamps to seasonal floodplains, riparian woodlands, and dry woodlands. This level of species diversity is normal for the southern African region, and all analyzed aquatic groups are composed of ubiquitous species with an additional significant proportion of species originating from northern, more tropical systems. Cyclical variations in climate over thousands of years have created a huge wetland complex in the upper Zambezi and Okavango Rivers during wet phases. This wetland complex has fragmented into the Okavango Delta and other large wetlands in Zambia during dry phases. There are no endemic species in the Okavango Delta while the South-central African wetland complex is a centre of endemism. Species diversity of the Okavango Delta is a consequence of this unique environment, with dynamic shifts in flooding patterns that in turn force constant changes in patterns of plant succession and dependent animals. Temporal variations in flooding also cause accumulation and sudden mobilization of nutrients which are readily used by well adapted plant species. As a consequence, locally high biological productivity occurs, which in turn results in high numbers of grazing mammals.
Species diversity of the Okavango Delta, Botswana (PDF Download Available). Available from: https://www.researchgate.net/publication/226358917_Species_diversity_of_the_Okavango_Delta_Botswana [accessed Nov 14 2017].