Kurzschwanz-Stachelschwein
Überordnung: EUARCHONTOGLIRES
Taxon ohne Rang: Nagetiere und Hasen (GLIRES)
Ordnung: Nagetiere (RODENTIA)
Unterordnung: Stachelschweinverwandte (Hystricomorpha)
Familie: Stachelschweine (Hystricidae)
Kurzschwanz- oder Malaiisches Stachelschwein
Hystrix brachyura • The Malayan Porcupine • Le porc-épic de Malaisie
- Körperbau und Körperfunktionen
- Verbreitung
- Lebensraum und Lebensweise
- Gefährdung und Schutz
- Bedeutung für den Menschen
- Haltung
- Taxonomie und Nomenklatur
- Literatur und Internetquellen
|
Weitere Bilder auf BioLib.cz |
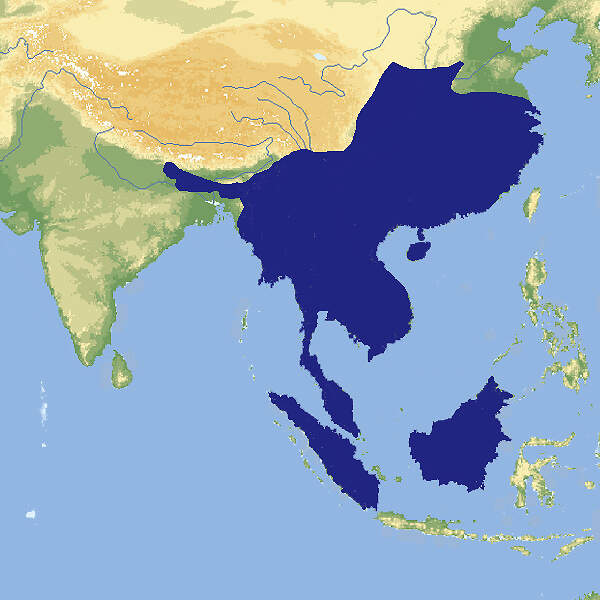
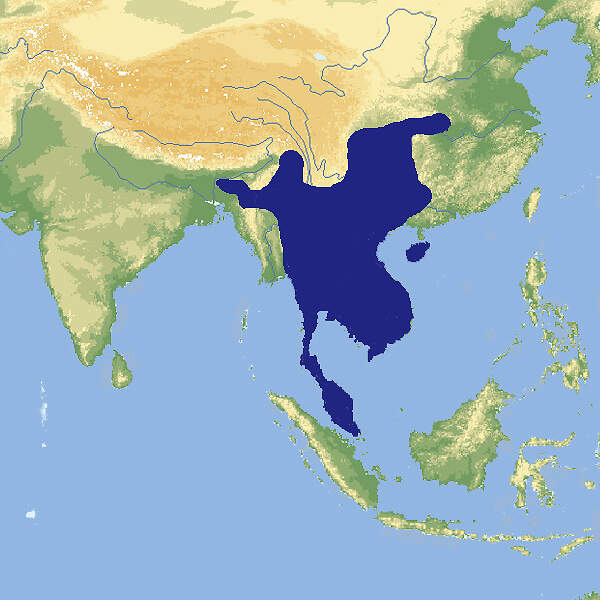
Die Vertreter der Gattung Hystrix sind wegen der Umwandlung des Haarkleids in ein Stachelkleid und wegen ihres Verhaltens von besonderem zoopädagogischem Interesse und gehören zu den Standardtieren in Zoologischen Gärten. Dies trifft allerdings für das nichtgefährdete, aus Südostasien stammende Kurzschwanz-Stachelschwein nicht zu. Dieses ist seit mehreren Jahrzenten aus europäischen Zoos verschwunden. Körperbau und KörperfunktionenKurzschwanz-Stachelschweine erreichen eine Kopf-Rumpflänge von 56-74 (45-93) cm, eine Schwanzlänge von 8-12 (6-17) cm und ein Gewicht von 10-18 (8-27) kg. Im Gegensatz zu dem auf dem Indischen Subkontinent ebenfalls vorkommenden Weißschwanzstachelschwein ist die Nackenmähne nur schwach ausgebildet, und die langen Rückenstacheln haben nur ein dunkles Querband und nicht mindestens drei [4]. VerbreitungSüdostasien: Bangladesch, Bhutan, Brunei (?), China, Hongkong, Indien, Indonesien, Laos, Malaysia, Myanmar, Nepal, Thailand, Vietnam [2]. Lebensraum und LebensweiseDas Kurzschwanz-Stachelschwein lebt in unterschiedlichen Waldtypen, mit Gestrüpp bedecktem, felsigem Gelände und auf Agrarland vom Meeresspiegel bis auf eine Höhe von 1'500 m. Die Tiere sind nachtaktiv und verschlafen den Tag einzeln oder familienweise in selbstgegrabenen Erdbauen. Sie fressen pflanzliches Material aller Art und benagen zur Deckung ihres Kalziumbedarfs Knochen und Abwurfstangen von Hirschen. Bei Gefahr rasseln sie mit dem Schwanz, und auch sonst entspricht das Feindvermeidungsverhalten dem der anderen Arten der Gattung. Nach einer Tragzeit von ca. 110 Tagen werden ein- bis zweimal im Jahr 2 oder gelegentlich 3 weitentwickelte Jungtiere geboren, deren Körper mit noch weichen Stacheln bedeckt ist [2; 4; 7]. Gefährdung und SchutzDie Art ist weitverbreitet, kommt in zahlreichen Schutzgebieten vor und gilt daher seit 2008, letztmals überprüft 2016, trotz angenommenem negativem Bestandstrend als nicht-gefährdet (Rote Liste: LEAST CONCERN). Es ist zu beachten, dass der Status der Art wegen ihrer heimlichen, nächtlichen Lebensweise schwer zu beurteilen ist. So wurde das Vorkommen in Bangladesch erst 2018 bestätigt, und in Singapur, wo die Art von 1970-2000 als möglicherweise ausgestorben galt, gibt es zahlreiche Nachweise, seit Fotofallen zur Überwachung der Wildbestände eingesetzt werden [1; 2; 5]. Der internationale Handel wird durch CITES nicht geregelt. Bedeutung für den MenschenDas Kurzschwanz-Stachelschwein wird zur Gewinnung von Fleisch und von Körperteilen für die Zwecke der traditionellen chinesischen Medizin bejagt und als Schädling an landwirtschftlichen Kulturen verfolgt [2]. Kulturelle Bedeutung: Der deutsche Dichter Christian MORGENSTERN (1871-1914) hat dem Kurzschwanz-Stachelschwein in seinen erstmals 1905 von Bruno CASSIRER verlegten "Galgenliedern" (1952) ein skurriles literarisches Denkmal gesetzt: DIE HYSTRIX
HaltungWEIGL gibt als längste Haltungsdauer 27 Jahre und 3 Monate an, erreicht von einem aus Sumatra importierten Wildfangs des Washingtoner Zoos [5]. Haltung in europäischen Zoos: In den 1960-80er Jahren wurde die Art in etwa einem halben Dutzend Zoos gehalten, darunter Berlin, Dresden, Halle Rostock und Schwerin [3]. Seitdem gibt es keine mehr. Die britische und vermutlich europäische Erstzucht glückte 1914 im Londoner Zoo. Für Details siehe Zootierliste. Nach Säugetiergutachten 2014 können Stachelschweine der Gattung Hystrix ganzjährig in Außengehegen gehalten werden, wenn sie im Winter Zugang zu einem frostfreien Schutzraum haben. Für 2 Stachelschweine soll eine Mindestfläche von 20 m² angeboten werden, für jedes weitere Tier 5 m² mehr. Die Schweizerische Tierschutzverordnung (Stand 01.06.2022) schreibt für 2 Stachelschweine ein Außengehege mit einer Mindestfläche von 40 m², Grabgelegenheit und Schlafboxen, eventuell heizbarem Innenraum vor. Nach der 2. Tierhaltungsverordnung Österreichs (Stand 2021) ist für ein Paar oder eine Familiengruppe Stachelschweine ein Außengehege mit einer Mindestfläche von 40 m² mit einer Sand- oder Erdschicht als Bodengrund und Unterstand erforderlich. Taxonomie und NomenklaturDas Kurzschwanz-Stachelschwein wurde 1758 von Carl von LINNÉ unter seinem heute noch gültigen Namen erstmals wissenschaftlich beschrieben. Der französische Naturforscher und Direktor der Ménagerie von Paris, Georges-Frédéric CUVIER, stellte es 1823 in die Gattung Acanthion, die heute als Untergattung betrachtet wird. Bis vor einiger Zeit wurden fünf Unterarten akzeptiert, gegenwärtig sind es noch deren drei [3; 7; 8]:
|
Literatur und Internetquellen
- CHUNG, Y. F., LIM, N. T.-L., SHUNARI, M. & WANG, D. (2016)
- LUNDE, D., APLIN, K. & MOLUR, S. (2016). Hystrix brachyura (errata version published in 2017). The IUCN Red List of Threatened Species 2016: e.T10749A115099298. https://dx.doi.org/10.2305/IUCN.UK.2016-3.RLTS.T10749A22232129.en. Downloaded on 23 November 2021.
- RUDLOFF, K. (2011)
- SMITH, A. T. & XIE, Y. (Hrsg., 2008)
- UL HASAN, M. A. & NEHA, S. A. (2019)
- WEIGL, R. (2005)
- WILSON, D. E. et al. eds. (2009-2019)
- WILSON, D. E. & REEDER, D. M. (2005)
Zurück zu Übersicht Hasen und Nagetiere
Weiter zu Weißschwanzstachelschwein (Hystrix indica)
Asiatischer Quastenstachler
Überordnung: EUARCHONTOGLIRES
Taxon ohne Rang: Nagetiere und Hasen (GLIRES)
Ordnung: Nagetiere (RODENTIA)
Unterordnung: Stachelschweinverwandte (Hystricomorpha)
Familie: Stachelschweine (Hystricidae)

Asiatischer Quastenstachler
Atherurus macrourus • The Asiatic Brush-tailed Porcupine • L'athérure malais
- Körperbau und Körperfunktionen
- Verbreitung
- Lebensraum und Lebensweise
- Gefährdung und Schutz
- Bedeutung für den Menschen
- Haltung
- Taxonomie und Nomenklatur
- Literatur und Internetquellen
|
Weitere Bilder auf BioLib.cz |
Der nicht-gefährdete Asiatische Quastenstachler ist ein kleines, langschwänziges Altwelt-Stachelschwein aus Südostasien, dessen Aussehen weniger spektakulär ist als jenes der Hystrix-Stachelschweine. In europäischen Zoos wurde er letztmals in den 1990er-Jahren gezeigt. Körperbau und KörperfunktionenMit einer Kopf-Rumpflänge von 38-52 (34-58) cm und einem Gewicht von 2-4 (1.5-4.3) kg ist der Asiatische Quastenstachler deutlich kleiner als die Stachelschweine der Gattung Hystrix. Sein Schwanz ist jedoch mit 16-20 (14-23) cm gleich lang oder länger als bei seinen großen Verwandten. Die Tiere sind relativ schlank und kurzbeinig. Hals, Schultern und Unterseite sind von teils schwarz- oder hellbraunen, teils weißlichen, weichen und abgeflachten Stacheln bedeckt. Die hintere Rückenpartie und die Flanken weisen bis 10 cm lange, grobe und längsgefurchte, harte Stacheln gemischt mit langen weißen Borsten auf. Der schuppige Schwanz endet in einer Quaste aus weißlichen, etwa 20 cm langen Stacheln. Die Weibchen haben im Brustbereich 2-3 Paare seitlich angelegter Zitzen [1; 4; 6]. VerbreitungSüdostasien: Bangladesch, China (Yunnan, Hainan, Hubei, Sichuan), Indien (Assam), Laos, Malaysia, Myanmar, Thailand, Vietnam [2]. Lebensraum und LebensweiseDer Quastenstachler ist eine nachtaktive, bodenlebende Art tropischer und subtropischer Bergwälder, vorzugsweise mit dichtem Unterwuchs und eingestreuten Zuckerrohr- und Bambusbeständen sowie Palmen. Als Unterkunft graben die Tiere Erdbaue, in denen sich bis zu 8 Individuen aufhalten können. Die Nahrung besteht aus Wurzeln, Knollen, Früchten, Baumrinde, Sämereien und anderem Pflanzenmaterial. Daneben werden auch Aas und Insekten genommen und Knochen angenagt. Die Weibchen gebären nach einer Tragzeit von 100-110 Tagen bis zweimal pro Jahr ein schon weit entwickeltes Junges, selten zwei. Dies verlässt das Nest, sobald die Stacheln ausgehärtet sind, was nach etwa einer Woche der Fall ist, und wird mit etwa 2 Monaten entwöhnt [1; 2; 4; 6]. Gefährdung und SchutzDie Art nimmt zwar in ihrem Bestand etwas ab, ist aber weitverbreitet und kommt in zahlreichen Schutzgebieten vor. Sie gilt daher seit 1996, letztmals überprüft 2016 als nicht-gefährdet (Rote Liste: LEAST CONCERN) [2]. Der internationale Handel wird durch CITES nicht geregelt. Bedeutung für den MenschenDer Asiatische Quastenstachler wird zur Fleischgewinnung bejagt [2]. HaltungWEIGL gibt als Höchstalter 13 Jahre und 7 Monate an, erreicht von einem vor dem 2. Weltkrieg im Londoner Zoo gehaltenen Tier. Tatsächlich dürfte das mögliche Höchstalter wie bei Atherurus africanus bei über 20 Jahren liegen [5]. Haltung in europäischen Zoos: Die Art war weltweit in Zoos stets selten, zu den wenigen Haltungen gehörte in den 1960er Jahren der Bergzoo Halle [3]. In Europa wurde sie letztmals bis 1995 im Tiergarten Schönbrunn gezeigt. Im Gegensatz dazu halten einige Zoos den Afrikanischen Quastenstachler. Die britische und vermutlich auch europäische Erstzucht glückte 1924 im Londoner Zoo. Für Details siehe Zootierliste. Nach Säugetiergutachten 2014 soll für 2 Tiere eine Mindestfläche von 10 m² angeboten werden, für jedes weitere Tier 2 m² mehr. Das Gutachten von 1996 sah für maximal 2 Tiere eine Mindestfläche von 5 m² vor. Die Erhöhung war zwar nicht wissenschaft abgestützt, war aber aus Sicht der Zoovertreter in Ordnung. Die Schweizerische Tierschutzverordnung (Stand 01.06.2022) schreibt für maximal 2 Tiere ein Innengehege mit einer Mindestfläche von 5 m² vor, wobei bei Neubauten allfällige neue Erkenntnisse berücksichtigt werden sollten. Nach der 2. Tierhaltungsverordnung Österreichs (Stand 2023) ist für ein Paar ein Gehege mit einer Mindestfläche von 15 m² erforderlich. Während der kalten Jahreszeit müssen die Tiere bei einer Mindesttemperatur von 18ºC gehalten werden. Taxonomie und NomenklaturDas Asiatische Quastenstachler wurde 1758 von Carl von LINNÉ als "Hystrix macroura" erstmals wissenschaftlich beschrieben. Der Gattungsname Atherurus wurde 1829 von dem französischen Naturforscher und Direktor der Ménagerie von Paris, Georges-Frédéric CUVIER, eingeführt. Die Art gilt als monotypisch, manche Autoren anerkennen allerdings zwei Unterarten [6]. |
Literatur und Internetquellen
- ANIMAL DIVERSITY WEB
- MOLUR, S. (2020). Atherurus macrourus (amended version of 2016 assessment). The IUCN Red List of Threatened Species 2020: e.T2354A166518819. https://dx.doi.org/10.2305/IUCN.UK.2020-1.RLTS.T2354A166518819.en. Downloaded on 22 November 2021.
- RUDLOFF, K. (2011)
- SMITH, A. T. & XIE, Y. (Hrsg., 2008)
- WEIGL, R. (2005)
- WILSON, D. E. et al. eds. (2009-2019)
Zurück zu Übersicht Hasen und Nagetiere
Weiter zu Südafrikanisches Stachelschwein (Hystrix africaeaustralis)
BAVEJA, P., TANG Q., LEE, J.G.H. & RHEINDT, F. (2019)
Impact of genomic leakage on the conservation of the endangered Milky Stork.
Biological Conservation 229(e1400253). DOI:10.1016/j.biocon.2018.11.009
Siehe auch Zeitungsartikel: https://www.eurekalert.org/news-releases/623399
Abstract:
Endangerment and extinction of threatened populations can often be accelerated by genomic contamination through infiltration with alien alleles. With a growing anthropogenic footprint, many such hybridization events are human-mediated. The Milky Stork (Mycteria cinerea) is one such species whose genomic composition is threatened by human-mediated hybridization with its sister taxon, the Painted Stork (Mycteria leucocephala). A comprehensive investigation of the stork population in Singapore using three complementary population-genomic approaches revealed a large proportion of hybrids that have undergone several generations of genomic leakage from Painted Storks and fall along a genetic cline that closely mirrors a phenotypic cline from pure Milky to pure Painted. Although originating from a limited number of introduced Painted Storks, these hybrids are now an integral part of both the wild and captive Singaporean and southern peninsular Malaysian stork population. Genetically informed conservation management including the isolation of hybrids in captivity and a strict removal of hybrids from the wild along with a release of genetically pure Milky Storks is imperative for continued survival. Similar approaches must become routine in endangered species conservation as human-mediated hybridization increases in volume.
bajeva biblio
ISMAIL, A., RAHMAN, F. (2016)
Current Status of the Milky Stork Re-introduction Programme in Malaysia and Its Challenges.
Trop Life Sci Res. 27(2): 13–24. doi: 10.21315/tlsr2016.27.2.2
Abstract:
This review discussed the current status of the Milky Stork Re-introduction Programme in Malaysia and the challenges it faced. Although it has continued for almost seven years, more challenges appeared as time elapsed mainly due to the arising conflicts between the implementation of conservation policy versus the development projects in Kuala Gula. Hence, the released population is struggling to adapt mainly due to the reduction of suitable habitat for nesting and disturbed foraging areas by the continuous anthropogenic activities. Furthermore, the lack of appropriate training among captive storks prior to being released also slows the adaptation of the birds in their new habitat. The increasing pattern of pollution in the area is also highlighted. Several suggestions were given to help improve the current re-introduction programme. These include improvements to the captive training method, improvement of the existing enclosure’s condition and environment, protection of remaining mangrove forest, creation of a buffer zone to mitigate the increasing pollution level in the area, close monitoring of the released population, and maintaining continuous support and awareness among the public. Considering the ongoing anthropogenic activities that may impair the status of Kuala Gula as an important bird sanctuary, emphasis should be given to achieve sustainable development throughout the area.
ismail-biblio
ISMAIL, A., RAHMAN, F., KIN, D. K. S., RAMLI, M. N. H. & NGAH, M. (2011)
Current Status of the Milky Stork Captive Breeding Program in Zoo Negara and its Importance to the Stork Population in Malaysia.
Tropical Natural History 11(1): 75-80.
Auszug:
The Malaysian government has the intention to increase the Milky Stork numbers and to this end several actions have been taken, such as a Milky Stork captive breeding and reintroduction program. With the support from both government and non-government agencies the first actual captive breeding and reintroduction program was done between 1998 and 2004 in Kuala Selangor Nature Park. The effort however had failed due to several problems and constraints. The program continues today in Kuala Gula, Perak. Before such initiative was taken, the captive breeding program in Zoo Negara was given less priority in solving the Milky Stork issue. After the first reintroduction in Kuala Selangor Zoo Negara focusses on the captive breeding for conservation purposes. This paper aims to analyse and report the Milky Stork breeding program in Zoo Negara and its success.
ismail-biblio
WASS Sachsenhagen: Bestandsstützung Wechselkröte
Aufzucht und Wiederansiedlung von Wechselkröten durch die Wildtier- und Artenschutzstation Sachsenhagen
Literatur und Internetquellen
- NESSMANN, M. (2020) Wechselkröten (Bufo viridis) - die letzten ihrer Art in Niedersachsen. Poster DGHT-Tagung 2020.
- ÖNSA - Pressemitteilung vom 27.08.2019.
- WILDTIER- UND ARTENSCHUTZSTATION SACHSENHAGEN
Zurück zu Schutz für heimische Amphibien
THALMANN, S., PECK, S., WISE, P., POTTS, J. M., CLARKE, J. & RICHLEY, J. (2015)
Translocation of a top-order carnivore: tracking the initial survival, spatial movement, home-range establishment and habitat use of Tasmanian devils on Maria Island.
Australian Mammalogy 38(1) 68-79.
Abstract:
The Tasmanian devil (Sarcophilus harrisii) is a carnivorous marsupial threatened with extinction from the emergence of Devil Facial Tumour Disease. The establishment of ex situ populations is a key management action for the species. We examined the initial survival, movement pattern, home range, and habit use of six devils from a total of 15 individuals translocated to Maria Island (south-east Tasmania). A total of 14 devils (93%) survived the initial monitoring phase within this study (122 days after translocation). The maximum and minimum distance recorded during one night was 21.73 km (range = 14.12–25.40 km) and 1.94 km (range = 0.07–7.71 km), respectively, while the average nightly distance travelled varied significantly (range = 7.24–13.07 km) between individuals. Short-term home-range size (90% kernel) varied from 936 to 3501 ha, with an average of 2180 (±836) ha for all devils. The habitat preference of devils on Maria Island shows a positive association with agricultural and urban habitats, and an avoidance of wet eucalypt forest. The home range and habitat associations may change as competitive pressures increase with population growth; however, this initial research indicates that translocation as a management action is a powerful tool for the establishment of ex situ populations, assisting in the continued conservation of this species.
thalmann-biblio
WEYRICH, H., BAUMGARTNER, H., HEGGLIN, D. & LÖRCHER, F. (2021)
Der Bartgeier - Seine erfolgreiche Wiederansiedlung in den Alpen.
248 Seiten, 206 Fotos, 2 Tabellen. Haupt Verlag Bern.
Beschreibung:
Als «Lämmergeier» verhasst, hatte es der Bartgeier in den vergangenen Jahrhunderten nicht leicht: Er wurde mit allen Mitteln gejagt und schlussendlich ausgerottet. Heute wissen wir, dass sich der Bartgeier nicht von Lämmern ernährt, sondern fast ausschließlich von Knochen. In den 1970er-Jahren begannen enthusiastische Bartgeierfreunde, die Wiederansiedlung zu organisieren - 1991 wurde die erste Auswilderung in der Schweiz unternommen. Heute, 30 Jahre später, steht fest, dass die Auswilderung von Bartgeiern eines der erfolgreichsten Auswilderungsprojekte im Alpenraum ist.
Ein Grund zum Feiern und für eine aktuelle Monografie über den größten Vogel des Alpenraums.
Mit atemberaubenden Bildern des Naturfotografen Hansruedi Weyrich.
weyrich-biblio
Zoos setzen sich für heimische Amphibien ein
|
|
Amphibien übernehmen wichtige Aufgaben in ihrem Ökosystem. Sie sind ein bedeutender Teil der Nahrungskette. In ihr Beuteschema fallen Schnecken und Insekten wie Mücken. Sie selbst wiederum sind wichtige Beutetiere für verschiedene Vögel, Reptilien und Säugetiere. Vielfach sind aber i9hre Lebensräume bedroht. Im Rahmen des vom Weltzooverband 2008 ausgerufenen Jahrs des Frosches sowie des Jahres der Biodiversität 2010 waren die Anstrengungen der Zoos, Tier- und Wildparks in Deutschland, Österreich und der Schweiz zu Förderung der lokalen Biodiversität durch Wiederherstellen und Unterhalten von Lebensräumen für Amphibien besonders bemerkenswert. In besonderen Fällen wurde auch die Wiederansiedlung lokal ausgestorbener Arten, wie des Kammmolchs oder des Laubfroschs angegangen. Dazu arbeiteten die Zoos eng mit lokalen Naturschutzorganisationen und Behörden zusammen. Das Herrichten und der Unterhalt von Amphibienbiotopen geschah oft im Rahmen von Aktionstagen mit Hilfe von Schulklassen, Zoo- und Naturfreunden als freiwilligen Helfern. Dabei handelte es sich um nachhaltige Maßnahmen, denn in der Regel bestehen diese Biotope heute noch. Indirekte Massnahmen zum Schutz einheimischer Amphibien waren von konkreten Projekten losgelöste PR-Aktionen, wie "Der Lurch des Jahres" der DGHT, sowie Forschungsarbeiten. Im Rahmen der Amphibienkampagne der EAZA sammelten Zoos 410'803 € zur Unterstützung von in situ-Projekten. Weitere über 40'000 € kamen 2008/2009 für das Schutzprogramm der Zoos, Tier- und Wildparks im deutschsprachigen Raum zusammen. Koordiniert durch den Verband der Zoologischen Gärten (VdZ) konnte dieses bis 2016 Projektförderungen im Umfang von 192'668 € vergeben. Ab dann wurde das Programm durch die Stiftung Artenschutz verwaltet. |
Beispiele
| Zoo Augsburg | Patenschaft für Laubfrosch-Biotop | ...mehr |
| Zoo Augsburg | Amphibien-Lebensraum im Zoo | ...mehr |
| Tierpark Bischofswerda | Erhalten eines Amphibienbiotops | ...mehr |
| Aquazoo Düsseldorf | Lebensraum für Amphibien schaffen | ...mehr |
| Natur- und Tierpark Goldau | Wiederansiedlung des Laubfroschs | ...mehr |
| Natur- und Tierpark Goldau | Schaffen neuer Lebensräume im Park | ...mehr |
| Kölner Zoo | Amphibienschutz im Nüssenberger Busch | ...mehr |
| Kölner Zoo | Regionale Erhaltung der Wechselkröte |
...mehr |
| Kölner Zoo | Information und Laichbiotop im Zoo | ...mehr |
| Zoo Landau | Aufwertung eines Teichgebiets | ...mehr |
| Vogelpark Marlow | Ein Platz für Frösche | ...mehr |
| Tierpark Nordhorn | Wir helfen Fröschen und Kröten | ...mehr |
| Tiergarten Nürnberg | Zucht und Wiederansiedlung | ...mehr |
| Tiergarten Schönbrunn | Sichere Amphibienwanderung | ...mehr |
| Tiergarten Schönbrunn | Amphibienkartierung | ...gesperrt |
| Tiergarten Straubing | Zucht und Ansiedlung von Gelbbauchunken |
...mehr |
| Zoo Wuppertal | Schutz der Geburtshelferkröte | ...mehr |
| Wildnispark Zürich-Langenberg | Amphibienschutz im Wildnispark | ...mehr |
| Wildpark Eekholt | Bildungsarbeit mit Amphibien | ...mehr |
Zurück zu Lurche (Amphibia)
WOODFINE, T., WILKIE, M., GARDNER, R., EDGAR, P., MOULTON, N. & RIORDAN, P. (2017)
Outcomes and lessons from a quarter of a century of Sand lizard Lacerta agilis reintroductions in southern England.
Int. Zoo Yearb. 51: 87-96. https://doi.org/10.1111/izy.12155
Volltext (PDF)
Abstract:
Despite occurring widely across Europe and Asia, the Sand lizard Lacerta agilis is threatened in the north-western part of its range and had disappeared from much of its former habitat in England and Wales prior to concerted conservation action. A breeding population established at Marwell Zoo, UK, contributed to the re-establishment of 26 populations of Sand lizards at heathland and coastal dune sites across southern England as part of a wider multi-stakeholder response to reverse the decline of the species. Knowledge about the biology of Sand lizards was accrued during the process, which helped to refine the management of the breeding population that was maintained in a naturalistic setting within the indigenous range of the species. These successes were underpinned by coordinated collaborative actions and long-term institutional commitments against a backdrop of considerable change in the statutory framework governing Sand lizard conservation. The management of this project was not without cost or risk, including protection of valuable founder stock, incomplete knowledge about the health and disease status of Sand lizards, intrinsic constraints of limited founder representation, and the challenges of monitoring this elusive species post release.
woodfine-biblio