LAVILLA, E. O., LANGONE, J. A., PADIAL, J. M. & DE SÁ, R. O. (2010)
The identity of the crackling, luminescent frog of Suriname (Rana typhonia Linnaeus, 1758) (Amphibia, Anura).
Zootaxa 2671: 17–30 (9 Nov. 2010) 1 plates; 97 references
Abstract:
Review of the literature and recently available field notes from the collector of the type allows a reconsideration of the identity of the Linnaean name Rana typhonia. We provide evidence to demonstrate that the Linnaean species is neither a bufonid nor an Asiatic ranid, but a Neotropical hylid. Subsequently, we consider Rana typhonia as an older synonym of Rana venulosa Laurenti, 1768, redescribing its holotype under the new combination, Trachycephalus typhonius (Linnaeus, 1758).
PYRON, R. A. & WIENS, J. J. (2011)
A large-scale phylogeny of Amphibia including over 2800 species, and a revised classification of advanced frogs, salamanders, and caecilians.
Molecular Phylogenetics and Evolution 61: 543–583.
Volltext (Link)
Abstract:
The extant amphibians are one of the most diverse radiations of terrestrial vertebrates (>6800 species). Despite much recent focus on their conservation, diversification, and systematics, no previous phylogeny for the group has contained more than 522 species. However, numerous studies with limited taxon sampling have generated large amounts of partially overlapping sequence data for many species. Here, we combine these data and produce a novel estimate of extant amphibian phylogeny, containing 2871 species (40% of the known extant species) from 432 genera (85% of the 500 currently recognized extant genera). Each sampled species contains up to 12,712 bp from 12 genes (three mitochondrial, nine nuclear), with an average of 2563 bp per species. This data set provides strong support for many groups recognized in previous studies, but it also suggests non-monophyly for several currently recognized families, particularly in hyloid frogs (e.g., Ceratophryidae, Cycloramphidae, Leptodactylidae, Strabomantidae). To correct these and other problems, we provide a revised classification of extant amphibians for taxa traditionally delimited at the family and subfamily levels. This new taxonomy includes several families not recognized in current classifications (e.g., Alsodidae, Batrachylidae, Rhinodermatidae, Odontophrynidae, Telmatobiidae), but which are strongly supported and important for avoiding non-monophyly of current families. Finally, this study provides further evidence that the supermatrix approach provides an effective strategy for inferring large-scale phylogenies using the combined results of previous studies, despite many taxa having extensive missing data.
pyron-biblio
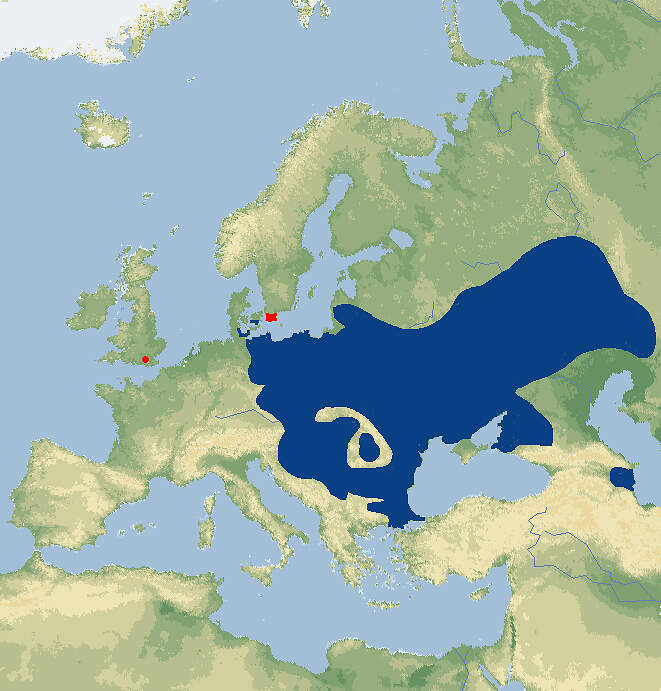
Rotbauchunke
Ordnung: Froschlurche (Anura)
Unterordnung: Urfrösche (Archaeobatrachia)
Familie: Unken (Bombinatoridae)
Rotbauchunke
Bombina bombina • The Fire-bellied Toad • Le sonneur à ventre de feu
beginn
- Körperbau und Körperfunktionen
- Verbreitung
- Lebensraum und Lebensweise
- Gefährdung und Schutz
- Bedeutung für den Menschen
- Haltung
- Taxonomie und Nomenklatur
- Literatur und Internetquellen
|
Weitere Bilder auf BioLib
|
Als im Terrarium gut zu beobachtende einheimische Art ist die regional gefährdete Rotbauchunke eine gute Botschafterart für Amphibienschutz vor der Haustür. Sie wird daher öfter im Zoo gezeigt, allerdings nicht so häufig wie ihre sehr ähnliche Verwandte aus China. Körperbau und KörperfunktionenRotbauchunken erreichen eine Kopf-Rumpflänge von 45-55 mm. Männchen und Weibchen sind etwa gleich groß. Mitteleuropäische Tiere bleiben meist etwas kleiner. Kopf und Körper sind abgeflacht, der Körper etwas schlanker als bei der Gelbbauchunke. Die nahe beisammenstehenden Augen haben herzförmige Pupillen mit nach unten gerichteter Spitze. Das Trommelfell ist nicht sichtbar, Parotoiddrüsen fehlen, dagegen befindet sich im Nacken ein paarig angeordneter, bogenförmiger Drüsenkomplex. Die Haut ist mit vielen flachen Warzen mit kleinen schwarzen Hornstacheln besetzt. Die Oberseite ist hell- bis dunkelgrau gefärbt oder bräunlich mit dunklen Flecken, teilweise kommen auch grüne Individuen vor. Die Unterseite weist rote bis orange Flecken auf schwarzem bis dunkelgrauem, mit kleinen weißen Pünktchen durchsetztem Grund auf [4; 6]. Im Gegensatz zur Gelbbauchunke haben männliche Rotbauchunken Schallblasen, und ihr Ruf ist deshalb lauter. Während der Paarungszeit weisen sie dunkle Brunstschwielen an den Unterarmen und den ersten beiden Fingern auf [5]. VerbreitungEuropa: Weit verbreitet in den tieferen Lagen Mittel- und Ost-/Südosteuropas: Bosnien und Herzegowina, Bulgarien, Dänemark, Deutschland, Griechenland, Kasachstan, Kroatien, Lettland, Litauen, Moldawien, Österreich, Polen, Rumänien, Russland, Serbien, Slowakei, Slowenien, Tschechien, Türkei, Ukraine, Ungarn, Weißrussland. Wiederangesiedelt in Südschweden, angesiedelt in Großbritannien (Surrey) [1; 6]. Lebensraum und LebensweiseLebensraumansprüche: Im Gegensatz zur Gelbbauchunke bevorzugen Rotbauchunken Gewässer mit reicher Unterwasservegetation. Der Wasserstand der Laichgewässer schwankt saisonal stark. Für eine erfolgreiche Aufzucht ist wichtig, dass sie gut besonnt und fischfrei sind und ausgedehnte Flachwasserzonen aufweisen. Der Landlebensraum kann bis zu 100 m vom Laichgewässer entfernt sein. Benötigt werden genügend Bodenfeuchtigkeit und Versteckmöglichkeiten unter Steinen, Totholz oder im Wurzelbereich von Bäumen oder Sträuchern [3; 4; 5]. Lebensräume: Rotbauchunken leben in offenen, Landschaften wie Steppen, Weiden, Wiesen, Ackerland, Überschwemmungsbereichen in Flussauen, lockeren Wäldern und warmen Waldrändern [3; 4; 5]. Biologie: Rotbauchunken ernähren sich von Regenwürmern, Nacktschnecken und Insekten. Bei Gefahr nehmen sie eine Warnstellung ein, bei der die Extremitäten über den Rücken genommen und der Rücken nach innen gekrümmt wird, sodass die bunte Unterseite sichtbar wird. Während der langen Fortpflanzungszeit von Ende April bis Juli und bisweilen bis August, legen die Weibchen bis zu 300 Eier, die in mehreren Laichbällchen im Gewässer verteilt an Wasserpflanzen geheftet werden. Die Larven schlüpfen nach 2-5 Tagen, die Metamorphose in 11-15 mm große Jungunken erfolgt nach 8-12 Wochen, je nach Wassertemperatur und Nahrungsangebot. Gelegentlich können die spät geschlüpften Larven auch überwintern [3; 4; 5; 6]. Gefährdung und SchutzDie Art ist weltweit nicht gefährdet. In Deutschland ist sie in neun Bundesländern heimisch und gilt insgesamt als stark gefährdet, in Hamburg und Thüringen ist sie ausgestorben und in Berlin und Niedersachsen vom Aussterben bedroht. In Österreich gilt sie als gefährdet, sie kommt nur vor in Wien, Niederösterreich, Burgenland, Steiermark sowie marginal in Oberösterreich. In der Schweiz ist die Art nicht heimisch [1]. Der internationale Handel ist nicht unter CITES geregelt. Die Rotbauchunke fällt unter Anhang 2 der Berner Konvention über die Erhaltung der europäischen wildlebenden Pflanzen und Tiere und ihrer natürlichen Lebensräume und ist in den Anhängen II und IV der FFH-Richtlinie (92/43/EWG) aufgeführt. Praktische Schutzmaßnahmen: Erhaltung und Unterhalt der Laichgewässer, Schaffen neuer Gewässer, Vernetzung der Lebensräume. Zoogestützte Schutzprojekte:Rotbauchunken profitieren von Schutzmaßnahmen der Zoos zugunsten der einheimischen Amphibien, namentlich von der Anlage und Pflege von Laichgewässern inner- und außerhalb der Zoos, z.B: Bedeutung für den MenschenVerängstigte Unken können ein nach Lauch riechendes Gift ausscheiden, das auch ohne direkte Berührung die Schleimhäute stark reizt, sodass einem z.B. die Augen tränen [5]. HaltungHaltung in europäischen Zoos: Die Art wird in gegen 20 europäischen Einrichtungen gezeigt, von denen sich über 40% im deutschsprachigen Raum befinden. Für Details siehe Zootierliste. Mindestanforderungen an Gehege: In Deutschland gibt es keine konkreten Mindestanforderungen. In Österreich sind diese in Anlage 4 der 2. Tierhaltungsverordnung, in der Schweiz in Anhang 2, Tabelle 6 der Tierschutzverordnung festgelegt. Taxonomie und NomenklaturCarl von LINNÉ nannte die Art 1761 "Rana bombina". Der österreichische Arzt und Naturforscher Josephus Nicolaus LAURENTI stellte sie 1768 als "Bufo igneus" zu den Kröten. 1820 wurde die Gattungsbezeichnung Bombinator eingeführt, durchgesetzt hat sich aber bis heute der vom Nürnberger Naturforscher und Kupferstecher Jacob STURM 1828 verliehene Gattungsname Bombina [2]. |
Literatur und Internetquellen
- AGASYAN, A. et al. (2009). Bombina bombina. The IUCN Red List of Threatened Species 2009: e.T2865A9489517. http://www.iucnredlist.org/details/2865/0. Downloaded on 12 December 2017.
- AMPHIBIAN SPECIES OF THE WORLD
- AMPHIBIAWEB
- FROSCHNETZ
- GRZIMEK, B. (Hrsg. 1970)
- NIETZKE, G. (1969)
Zurück zu Übersicht Zungenlose, Scheibenzüngler, Krötenfrösche
PINYA, S. & CARRETERO, M. A. (2011)
The Balearic herpetofauna: a species update and a review on the evidence.
Acta Herpetologica 6(1): 59-80, 2011
Abstract:
Here, we update the current list of amphibian and reptile fauna present in he Balearic Islands, probably the most outstanding case in the Mediterranean and of the most in the world where massive species introduction is in conflict with the survivorship,of highly restricted endemic taxa. Resulting of a long term evolution in insularity,endemic herpetofauna was already decimated during the Pleistocene but, after the human colonisation of the archipelago, the introduction of alien species, passive or deliberate, has been provoking new extinctions and range retractions in the native herpetofauna. Such process is not interrupted but has even intensified during the last years. The current species list is composed by five amphibians (one native) and 21 reptiles (2 native). A critical review of the evidence on extinctions and introductions is provided together with the conservation implications. Compared to the last review (Mayol, 1985) six new reptile species are now naturalised or are in process of naturalization, colubrid snakes constituting the most conflicting element due to their predator role.
pinya-biblio
GARCÍA, G. (2007)
Case report 7 - Montserrat mountain chicken (Leptodactylus fallax): Breeding, reintroduction and other conservation measures.
In: DOLLINGER, P. ed. (2007) Amphibien brauchen unsere Hilfe. Verhandlungsbericht des Amphiobienkurses gemeinsam organisiert mit den Zooverbänden im deutschsprachigen Raum. Chemnitz, 27.-30. Juni 2007. WAZA, Bern: S. 118.
Zusammenfassung der Powerpoint-Präsentation:
The mountain chicken is one of the most threatened amphibians in the world. Its range historically included up to seven, Eastern Caribbean islands but the species is now confined to the islands of Dominica and Montserrat. A combination of hunting, introduced predators and habitat loss was thought to have caused the extirpation of the species from the islands of Guadeloupe, St Kitts and Martinique around 500 years ago.
The wild populations on Montserrat were severely affected when the Soufriere Hills volcano erupted after a 350-year period of dormancy in 1995 and destroyed a significant part of its range. The species distribution on Montserrat has fallen to less than 17km2 and the increasingly toxic, acidified environment may have reduced juvenile survivorship and reproduction. The current status of the Montserrat population is unknown after renewed volcanic eruptions on 13th July 2003 covered the island in a thick layer of ash. Lately, 2005 and 2006 severe impact of the volcano affected the island again.
Chytrid fungus has been found on the populations of Mountain chickens in Dominica. Although no cases of chytrid disease have been reported in Montserrat, this island may also be at risk. If Montserrat is unaffected, frog populations on the island may be the last hope for the survival of the species.
In collaboration with the Government of Montserrat, Durrell Wildlife has initiated captive breeding of the species, and has also undertaken fieldwork to understand the animal in the wild.
We investigated the presence of disease on mountain chickens and the sympatric species within the Centre Hills in Montserrat. No chytrid or exposure to ranavirus was detected. We draw tentative conclusions about disease threats to the Montserrat mountain chicken population, and present preliminary recommendations for safeguarding this species.
A major biodiversity assessment effort led by Durrell, the Royal Society for the Protection of Birds (RSPB) and the Montserrat Government has been recently been completed and is aiding the management and declaration of the Centre Hills as a national park.
garcia-biblio
ROWLEY, J. J. L., SHEPERD, C. R., STUART, B. L., NGUYEN, T. Q., HOANG, H. D., CUTAJAR, T. P., WOGAN, G. O. U. & PHIMMACHAK, S. (2016)
Estimating the global trade in Southeast Asian newts.
Biological Conservation 199: 96-100. http://dx.doi.org/10.1016/j.biocon.2016.05.001
Abstract:
The global trade in amphibians is widespread, involves hundreds of species, and has been implicated in amphibian population declines. The pet trade is the primary driver for population declines in one Southeast Asian newt species (Laotriton laoensis), and is a known threat tomost of the 13 other knownspecies fromthe region. Despite this, there has been little attempt to assess the impact of collection for the pet trade on Southeast Asian newts.We examined available import data from the US, Europe and Hong Kong, assessed current online trade and surveyed local pet traders within Southeast Asia. Large numbers of Southeast Asian newts are harvested from the wild to meet the demands of the international pet trade, with more than 7500 individual newts imported into the US alone during 2005–2014. Internet trade surveys revealed the global extent of the trade, with Southeast Asian newts for sale as pets in 15 countries throughout Europe, Asia and North America, at between ~ USD30–260 each. The trade in newts within Southeast Asia appears negligible in comparison. Urgent measures are required in order to conserve Southeast Asian newts but the lack of data on the species and number of individuals impacted by the pet trade makes it difficult to monitor and accurately assess its threat. We strongly recommend that all Southeast Asian newts be listed on CITES. This measure should improve monitoring of trade and provides importing countries opportunity to curb trade in species that were illegally harvested, thus helping to safeguard wild populations.
CONWAY, W. G. (1973)
How to exhibit a bullfrog: a bed-time story for zoo men.
Int. Zoo Yearbook 13: 221-226.
Ganzer Artikel als PDF
PIENAAR, U. DE V. ; PASSMORE, N.I. & CARRUTHERS, V.C. (1976)
The Frogs of the Kruger National Park: A guide to a group of vertebrate animals known as Amphibia-order Anura (Salientia) of the Kruger National Park.
91 Seiten, Farbfotos und Verbreitungskarten aller 33 im Krüger-Nationalpark vorkommender Arten; kart.;
National Parks Board of Southa Africa, Pretoria. ISBN-10: 0869530186<, ISBN-13: 9780869530184.
pienaar-biblio
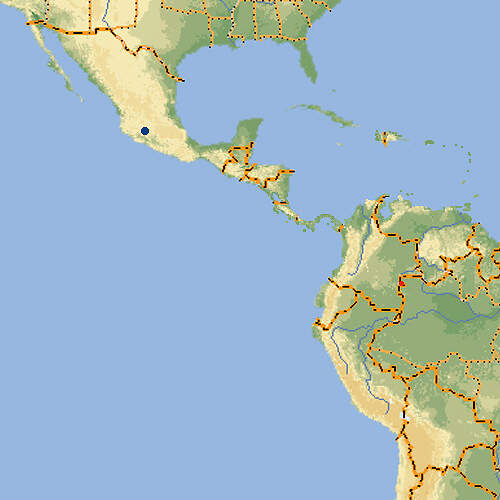
Pátzcuaro-Querzahnmolch
Ordnung: Schwanzlurche (Caudata)
Überfamilie: Salamanderverwandte (Salamandroidea)
Familie: Querzahnmolche (Ambystomatidae)
Pátzcuaro-Querzahnmolch
Ambystoma dumerilii • The Lake Patzcuaro Salamander • La salamandre du Lac Patzcuaro
- Körperbau und Körperfunktionen
- Verbreitung
- Lebensraum und Lebensweise
- Gefährdung und Schutz
- Bedeutung für den Menschen
- Haltung
- Taxonomie und Nomenklatur
- Literatur und Internetquellen
|
Weitere Bilder auf BioLib
|
Der Pátzcuaro-Querzahnmolch ist eine in ihrer Heimat vom Aussterben bedrohte Art, für die wegen ihres beschränkten Lebensraums der Aufbau von ex situ-Reservepopulationen wichtig ist. Körperbau und KörperfunktionenPátzcuaro-Querzahnmolche durchlaufen nie eine Metamorphose zum Erwachsenenstadium, sondern werden als Larven geschlechtsreif. Voll ausgewachsene Larven haben eine Kopf-Rumpflänge von etwa 165 mm und eine Schwanzlänge von 120 mm. Der Kopf ist groß, mit kleinen, lidlosen Augen und beidseits drei federartigen äußerlichen Kiemenästen. Der Körper ist relativ schlank mit einer flossenartigen Längsfalte auf dem Rücken. Der Schwanz ist seitlich zusammengepresst und hat oben wie unten einen Flossensaum. Die Extremitäten haben vorne 4, hinten 5 Zehen, die durch Schwimmhäute verbunden sind [2]. VerbreitungNordamerika: Mexiko, nur in einem kleinen Teil des 126 km² großen Pátzcuaro-Sees im Teilstaat Michoacán [4]. Lebensraum und Lebensweise
Wie der Axolotl erreicht der Pátzcuaro-Querzahnmolch seine Geschlechtsreife bereits im Larvenstadium, macht also keine Metamorphose zum Erwachsenenstadium durch. Dieses, Neotenie genannte Phänomen ist durch eine Unterfunktion der Schilddrüse bedingt. Er hat deshalb eine rein aquatische Lebensweise [4]. Gefährdung und SchutzDer Pátzcuaro-Querzahnmolch ist im Freiland hochgradig bedroht, vermutlich sogar ausgestorben. Da die letzte Beurteilung aus dem Jahr 2003 stammt, wird er von der IUCN noch als vom Aussterben bedroht taxiert. Heute ist davon auszugehen, dass die Pátzcuaro-Querzahnmolche im einzigen See, in dem sie natürlicherweise vorkamen, ausgestorben sind, weil Fische, die in den See eingesetzt wurden, ihre Eier und Larven gefressen haben. Außerdem wurde Abwasser eingeleitet und flache Uferbereiche aufgefüllt. Nonnen in einem nahegelegenen Kloster hatten Tiere gesammelt, um aus ihnen Hustensaft zu gewinnen. Sie haben sie bis vor Kurzem allerdings auch gezüchtet und somit hat die Art überlebt [5]. Der internationale Handel ist nach CITES-Anhang II geregelt. Bedeutung für den MenschenDie Art wurde für medizinische Zwecke genutzt, wobei die Sammeltätigkeit nicht nachhaltig war [4]. Von 2001-2016 wurde keine internationale Handelstätigkeit registriert [3], obwohl offensichtlich Nachzuchttiere aus Mexiko ausgeführt worden sind. HaltungHaltung in europäischen Zoos: Ein Österreichischer Forscher aus Graz hatte die Möglichkeit, ein paar Tiere aus Mexiko zu importieren und es gelang ihm, diese zur Zucht zu bringen. Aus seinem Bestand gingen einige Individuen an den Tiergarten Schönbrunn, dem 2015 die Zoo-Welterstzucht gelang [PM Tiergarten Schönbrunn vom 30.07.2015]. Mittlerweile ist die Art in rund zwei Dutzend europäischen Einrichtungen zu sehen, von denen sich etwa drei Viertel im deutschsprachigen Raum befinden. Für Details siehe Zootierliste. Es gibt jetzt auch ein Europäisches Erhaltungszuchtprogramm (New Style-EEP), das vom Chester Zoo koordiniert wird. 2021 wurden Leitlinien für eine gute Haltungspraxis herausgegeben. Mindestanforderungen an Gehege: In Deutschland gibt es keine konkreten Mindestanforderungen. In Österreich sind diese in Anlage 4 der 2. Tierhaltungsverordnung, in der Schweiz in Anhang 2, Tabelle 6 der Tierschutzverordnung festgelegt. Taxonomie und NomenklaturDie Art wurde 1870 von dem aus Frankreich stammenden mexikanischen Zoologen Alfred DUGÈS unter der Bezeichnung Siredon dumerilii beschrieben. 1889 stellte sie der amerikanische Zoologe Edward Drinker COPE in die bereits 1838 von dem Schweizer Naturforscher, Arzt und Diplomaten Johann Jakob von TSCHUDI aufgestellte Gattung Ambystoma [1]. |
Literatur und Internetquellen
- AMPHIBIAN SPECIES OF THE WORLD
- CITES IDENTIFICATION MANUAL
- CITES TRADE DATA BASE
- SHAFFER, H.B., FLORES-VILLELA, O., PARRA-OLEA, G. & WAKE, D. (2008). Ambystoma dumerilii. The IUCN Red List of Threatened Species 2008: e.T59055A11876338. http://www.iucnredlist.org/details/59055/0. Downloaded on 28 November 2017.
- TIERGARTEN SCHÖNBRUNN - PRESSEMITTEILUNG
Zurück zu Übersicht Schwanzlurche
Weiter zu Axolotl (Ambystoma mexicanum)
MOBARAKI, A., AMIRI, M., ALVANDI, R., TEHRANI, M.E., KIA, H.Z., KHOSHNAMVAND, A., BALI, A., FOROZANFAR, E. & BROWNE, R.K. (2014)
A conservation reassessment of the Critically Endangered, Lorestan newt Neurergus kaiseri (Schmidt 1952) in Iran.
Amphibian and Reptile Conservation 9 (1): 16- 25.
Abstract:
The Lorestan newt (Neurergus kaiseri, Schmidt 1952) is an endemic salamander species to Iran, listed as “Critically Endangered” in the 2006 IUCN Red List due to population declines of 80%, over collection for the pet trade; area of occupancy less than 10 km2, fragmented populations, less than 1,000 adults, and continuing habitat degradation and loss. However, the Red List assessment was limited to surveys only around the type location of N. kaiseri. We conducted a series of field surveys over the previously known region inhabited by N. kaiseri, and over some other areas that appeared to provide suitable habitat for N. kaiseri. Two Iranian provinces of Khuzestan and Lorestan were surveyed with 20 aquatic sites inhabited by N. kaiseri distributed over an area of ~10,000 km² that included 14 new sites, with 11 of these remote from previously recorded sites. We estimate a minimum total population of greater than ~9,000 adult N. kaiseri at the sites we surveyed. The total population of N. kaiseri is certainly considerably greater than 9,000, because we surveyed only a small area of the potential range of N. kaiseri, and because more breeding sites appear during exceptionally wet periods. We consider that N. kaiseri needs greater conservation planning and implementation, habitat and legal protection, and increasing support for the expansion of community conservation programs. Conservation initiatives for N. kaiseri will also benefit many other threatened species including the Iran cave barb (Iranocypris typhlops), spur-thighed tortoise (Testudo graeca), Persian leopard (Panthera pardus ciscaucasica), brown bear (Ursus arctus), Caucasian squirrel (Sciurus anomalus) and saker falcon (Falco cherrug). The information provided by our survey warrants a reassessment of the IUCN Red List conservation status of N. kaiseri. However, to guide this reassessment a conservation action plan should be prepared by the Department of the Environment of Iran, with contributions by Iranian and International experts on all facets of the conservation of Neurergus species especially including the expansion of community conservation programs.
mobaraki-biblio